nitriles (suite)
Les nitriles sont généralement liquides ; HCN bout à 28 °C ; il est miscible à l’eau en toutes proportions ; la solubilité dans l’eau des autres nitriles diminue lorsque la masse molaire augmente ; Φ—CN y est pratiquement insoluble. Les nitriles possèdent une odeur forte ; ils sont toxiques, mais moins que l’acide cyanhydrique. En infrarouge, la fonction nitrile est caractérisée par une bande forte vers 2 200 cm–1 (domaine des liaisons triples).
La liaison triple carbone-azote est fortement polarisée :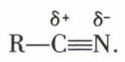
Cela fait prévoir des additions orientées, l’électrophile, pratiquement l’hydrogène ou un métal, s’additionnant à l’azote, tandis que le nucléophile s’unit au carbone ; ces additions peuvent se répéter dans le même sens :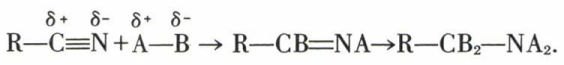
L’hydrogénation, catalytique ou chimique, conduit facilement à l’amine primaire R—CH2—NH2 ; toutefois, on passe par l’intermédiaire de l’imine R—CH=NH, qui peut être captée si l’on opère en milieu complexant (SnCl4) ; par hydrolyse de cette imine, on aboutit à l’aldéhyde R—CHO (réaction de Stéphan).
Les hydracides conduisent à des produits d’addition :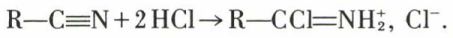
Ces chlorhydrates de chlorimines sont les intermédiaires probables d’autres additions réalisées en présence de HCl.
L’hydrolyse se passe en deux phases :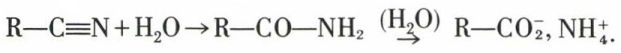
Lente en milieu neutre, elle est rapide en milieu acide, comme en milieu alcalin ; elle ne s’arrête au stade amide que si celui-ci est stériquement encombré.
À 0 °C, les alcools primaires engendrent des chlorhydrates d’iminoéthers, hydrolysables en esters :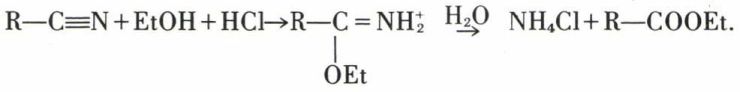
À température plus élevée, il se forme des orthoéthers :
Les aminés non tertiaires conduisent à des amidines :
Les hydrogènes liés au carbone, mais particulièrement actifs, s’unissent à l’azote ; avec le phénol :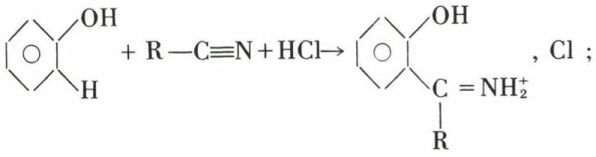
à l’hydrolyse, on recueille NH4Cl et une cétone-phénol.
Les organomagnésiens conduisent à des imidures, hydrolysables en cétones :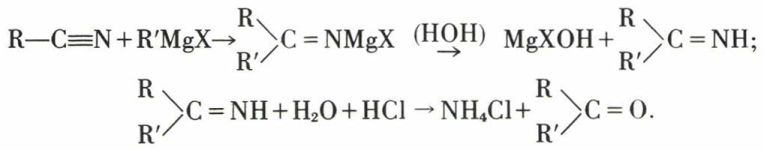
Mais l’hydrogène en α de —CN, s’il en existe, possède une certaine acidité ; d’où la réaction parasite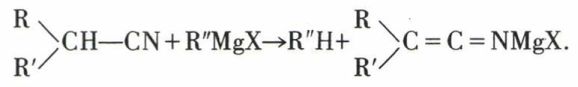
À l’hydrolyse, on trouve R″H et le nitrile de départ.
Les nitriles sont polymérisables ; s’il existe des hydrogènes en α de—CN, cette polymérisation est indéfinie et conduit à des résines ; dans le cas contraire, on observe une trimérisation irréversible :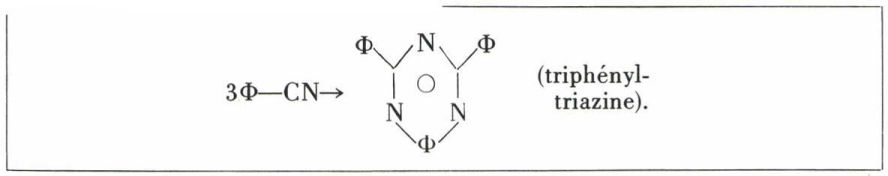
C. P.




