eau (suite)
Eaux industrielles
Leur évacuation peut souvent se faire, concurremment avec les effluents d’eaux usées, par les canalisations du domaine public, mais sous des conditions restrictives édictées par des règlements sanitaires.
M. D.
➙ Adduction / Agriculture / Aménagement du territoire / Aquatique / Aridité / Barrage / Boisson / Canal / Canalisation / Capillarité / Corrosion / Égout / Évaporation / Évapotranspiration / Fleuve / Glacier / Hydrologie et hydrographie / Hydrolyse / Lac / Neige / Océan / Pluie / Pollution / Prise et restitution / Réservoir / Soif / Tension superficielle / Thermalisme.
J. Gilbert et G. Bechmann, Traité d’adduction et de distribution d’eau (Dunod, 1919). / M. Cauvin, Cours de distribution d’eau et d’égouts (Eyrolles, 1947). / S. D. Faust et J. Unter, Principles and Application of Water Chemistry (New York, 1949). / P. J. Kramer, Plant and Soil Water Relationships (Londres, 1949). / Société académique Hütte, Des Ingenieurs Taschenbuch (Berlin, 1951-1955, 5 vol. ; trad. fr. Manuel de l’ingénieur, Béranger, 1960-1962, 2 vol.). / A. Builder, les Fosses septiques (Béranger, 1956). / P. Fourmarier, Hydrogéologie. Introduction à l’étude des eaux destinées à l’alimentation humaine et à l’industrie (Masson, 1958). / P. Koch, l’Alimentation en eau des agglomérations (Dunod, 1960). / M. Duriez et J. Arrambide, Nouveau Traité de matériaux de construction (Dunod, 1961-1962 ; 3 vol.). / C. Benezech, l’Eau, base structurale des êtres vivants (Masson, 1962). / R. Colas, la Pollution des eaux (P. U. F., coll. « Que sais-je ? », 1962 ; 2e éd., 1968). / C. Duval, l’Eau (P. U. F., coll. « Que sais-je ? », 1962). / H. Cambefort, Forages et sondages (Eyrolles, 1963). / T. R. Camp, Water and Its Impureties (New York, 1963). / G. Castany, Traité pratique des eaux souterraines (Dunod, 1963). / R. Furon, le Problème de l’eau dans le monde (Payot, 1963). / A. Cauvin et G. Didier, Distribution d’eau dans les agglomérations (Eyrolles, 1964). / J. L. Kavanau, Water and Solute-Water Interactions (San Francisco, 1964). / W. Fleischer et E. Fröhlich, l’Eau et les électrolytes dons l’organisme (trad. de l’all., Masson, 1965). / B. Dussart, Limnologie, l’étude des eaux continentales (Gauthier-Villars, 1966). / C. Gomella, la Soif du monde et le dessalement des eaux (P. U. F., 1966). / I. Chéret, l’Eau (Éd. du Seuil, 1967). / R. Colas, R. Labaud et P. Vivier, Dictionnaire technique de l’eau (le Prat, 1968). / M. Despax, la Pollution des eaux et ses problèmes juridiques (Libr. techniques, 1968). / M. Overman, Water (Londres, 1968 ; trad. fr. l’Eau dans le monde, Larousse, 1970). / J. Pimienta, le Captage des eaux souterraines (Eyrolles, 1971). / J. Bize, L. Bourguet et J. Lemoine, l’Alimentation artificielle des nappes souterraines (Masson, 1972). / R. Travers, l’Eau et l’homme (Maloine, 1973). / L. Legrand et G. Poirier, Chimie des eaux naturelles (Eyrolles, 1975).
L’eau dans le corps humain
Répartition de l’eau dans le corps
L’eau, qui constitue 70 p. 100 environ du poids du corps chez l’adulte, est répartie en compartiments définis par des différences anatomiques, biochimiques et fonctionnelles.
Le compartiment extra-cellulaire
Le compartiment extra-cellulaire comporte un secteur plasmatique (plasma sanguin) homogène, riche en protéines (70 g/l), de volume stable, et un secteur interstitiel, hétérogène (liquide céphalo-rachidien, lymphe, liquides articulaires). Ces deux secteurs sont séparés par la membrane vasculaire, perméable à l’eau et aux électrolytes mais non aux protéines.
Dans ce compartiment, le sodium représente 92 p. 100 des cations, et le CINa représente 240 mOsM/l pour une pression osmotique de 308 mOsM/l (mOsM est la millimole osmotique, millième de molécule-gramme [mole] responsable de la pression osmotique). Le potassium est un cation peu important.
Le compartiment cellulaire
Limité par la membrane des cellules, il est de composition variable selon les tissus. Ce compartiment, riche en protéines (50 mEq/l) et en potassium (100-150 mEq/l), est pauvre en sodium (10-15 mEq/l), en chlore (10 mEq/l) [mEq est le milli équivalent, millième de l’Eq, nombre d’atomes-grammes multiplié par la valence].
La membrane cellulaire
Elle maintient la différence de composition des deux secteurs hydriques, alors que les gradients de concentration tendent à la supprimer.
C’est une membrane de perméabilité sélective : elle est perméable aux électrolytes et surtout au sodium. Cette sélectivité exige une oxygénation correcte.
Le déséquilibre Na-K (entre sodium et potassium) s’explique par l’existence de la « pompe à sodium », mécanisme transportant activement hors de la cellule une quantité de sodium équivalant à celle que les gradients électriques et de concentration y font entrer, ainsi que par l’action inverse des gradients de concentration et électrique.
La membrane sépare donc des solutions de concentration osmotique totale identique, mais de composition différente.
Mesure des secteurs hydriques
On utilise les méthodes de dilution d’un indicateur. Cet indicateur est choisi en fonction du compartiment que l’on désire mesurer. Il doit s’y répartir uniformément et ne pas diffuser dans le secteur voisin.
Le volume du compartiment est donné par la formule 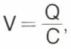 où Q est la quantité d’indicateur injectée et C sa concentration finale.
où Q est la quantité d’indicateur injectée et C sa concentration finale.
Les résultats chez l’adulte s’expriment par rapport au poids maigre : eau totale, 70 p. 100 ; eau plasmatique, 5 p. 100 ; eau cellulaire, 50 p. 100 ; eau interstitielle, 15 p. 100.
Chez le nourrisson, on a : eau totale, 77 p. 100 ; eau extra-cellulaire, 30 à 40 p. 100 du poids, la déshydratation survenant aisément.
Régulation du bilan hydrique
Besoins et pertes en eau
• Les pertes inévitables atteignent en moyenne (par jour) :
— urine 500 à 1 500 ml
— fèces 50 à 200 ml
— air expiré 400 à 600 ml
— sueur (sécrétion des glandes sudoripares) 100 ml à plusieurs litres
— perspiration (évaporation à travers la peau) 500 à 1 000 ml
• Les besoins sont de 30 à 40 ml/kg/j ; ils sont couverts par les boissons (1 litre ou plus), les aliments (1 litre) et l’eau endogène résultant des oxydations (300 ml).




