transformations thermodynamiques (suite)
Pour que la réversibilité soit complète, il nous faut étudier comment, dans cette transformation, peut être atteinte la réversibilité thermique. Deux solutions seulement se présentent. On peut supprimer les échanges de chaleur entre le gaz et le milieu extérieur en fabriquant toutes les parois (piston compris) avec des substances non absorbantes et non conductrices de la chaleur ; cet idéal, impossible à atteindre en raison des modes de transmission* de la chaleur, conduirait à une transformation adiabatique réversible, qu’on nomme aussi transformation isentropique, car elle n’est accompagnée d’aucune modification de l’entropie, ni du système, ni du milieu extérieur. On peut aussi permettre les échanges de chaleur, mais faire en sorte, pour éviter la création d’entropie, que ceux-ci ne s’effectuent qu’entre des corps à des températures aussi voisines que possible, ce qui suppose les parois conductrices (diathermanes) et, encore une fois, la transformation très lente ; on peut alors renverser le sens des échanges en modifiant infiniment peu, dans le sens convenable, la température du milieu extérieur ; là encore, la réversibilité se présente, pour le système et pour le milieu extérieur, comme une suite continue d’états d’équilibre ; on dira de cette transformation qu’elle est monotherme réversible ou isotherme.
Une transformation réelle est irréversible : il n’est pas possible à tout instant d’en renverser le sens par des modifications infiniment petites des paramètres qui définissent l’état du système ou celui du milieu extérieur, car les différences de température, de pression..., sont finies.
Les transformations réversibles offrent pour le raisonnement deux avantages importants.
1. Elles permettent l’emploi de représentations graphiques et de diagrammes*, puisque chaque état intermédiaire est bien défini et peut donc être représenté.
2. Elles permettent le calcul des échanges en fonction des paramètres d’état du système. C’est ainsi que le travail reçu par un gaz dans une compression ou une détente réversible s’écrit 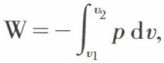 p étant la pression du gaz à chaque instant, v1 le volume initial et v2 le volume final. Si, en particulier, le gaz est parfait (pv = nRT), on a, pour une transformation isotherme,
p étant la pression du gaz à chaque instant, v1 le volume initial et v2 le volume final. Si, en particulier, le gaz est parfait (pv = nRT), on a, pour une transformation isotherme,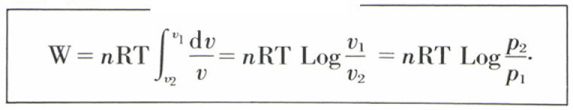
Si la transformation est isentropique, le gaz obéit à la loi de Laplace :
et, par suite,
ou encore :
On voit l’importance des transformations réversibles dans les raisonnements thermodynamiques. Toutefois, depuis quelques décennies se développe activement une thermodynamique* quantitative des transformations irréversibles qui doit permettre une approche à la fois plus cohérente et plus précise des phénomènes réels.
R. D.





