mercure
(latin scientifique médiéval mercurius, du latin classique Mercurius, nom propre)

Métal blanc très brillant, liquide à la température ordinaire. (Élément de symbole Hg.)
- Numéro atomique : 80
- Masse atomique : 200,59
- Masse volumique : 13,6 g/cm3
- Température de fusion : −38,87 °C
- Température d'ébullition : 356,58 °C
CHIMIE
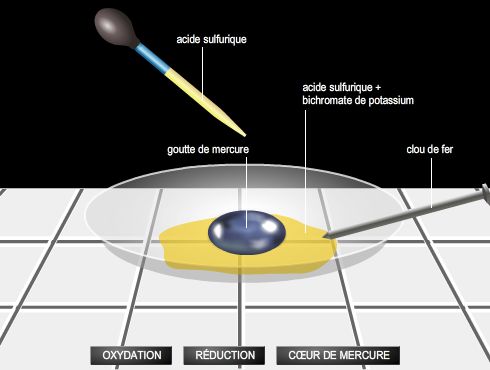
Élément assez volatil dont les vapeurs sont toxiques, le mercure possède une densité exceptionnellement élevée pour un liquide et une forte résistivité. Il dissout facilement l'or, l'argent, le plomb, les métaux alcalins, pour donner des alliages plus ou moins consistants, les amalgames. À l'air, il s'altère lentement, en se recouvrant d'une pellicule grise d'oxyde mercureux. À 350 °C, il s'oxyde plus rapidement, en donnant de l'oxyde mercurique rouge HgO. Il est attaqué par le chlore à froid, par le soufre à chaud ; il décompose l'acide sulfurique concentré et l'acide nitrique.
On obtient le mercure par grillage du cinabre (sulfure de mercure). On l'emploie dans la construction de thermomètres, baromètres, pompes à vide, lampes et redresseurs à vapeur de mercure, contacteurs ; il sert à l'étamage des glaces, à la fabrication de colorants, de fulminate de mercure, etc. Le mercure est monovalent (sous une forme Hg22+) dans les composés mercureux (oxyde Hg2O noir, chlorure Hg2Cl2 ou calomel) et divalent dans les composés mercuriques (oxyde HgO rouge ou jaune, chlorure HgCl2 ou sublimé corrosif, sulfure HgS, cinabre ou vermillon, fulminate Hg(OCN)2 employé comme détonateur dans les explosifs). Avec les radicaux aromatiques, le mercure donne des composés organométalliques.
La vapeur de mercure, excitée par une décharge électrique, produit une lumière verdâtre qui peut être amplifiée par photoluminescence (lampes fluorescentes). L'ajout à la vapeur d'halogénures métalliques permet de diversifier la couleur de la lumière (lampes aux halogénures).
ÉCOLOGIE
Les activités industrielles et l'utilisation des combustibles fossiles s'accompagnent d'importants déversements de mercure dans les milieux naturels. Introduit dans un cours d'eau lors d'une pollution, le mercure, pour partie, se volatilise dans l'atmosphère, puis retombe, à l'état natif, avec les pluies. Une autre partie, absorbée, directement ou indirectement, par les plantes et les animaux aquatiques, circule et se concentre fortement le long des chaînes alimentaires. En outre, l'activité microbienne transforme le mercure métallique en mercure organique hautement toxique. C'est ainsi que s'explique la forte teneur en thiométhyl-mercure des poissons de la baie de Minamata, au Japon, où une usine de produits chimiques déversait directement du mercure. La consommation de ces poissons entraîna le décès de 46 personnes dans un village de pêcheurs, de nombreux cas d'empoisonnement et de déficiences chez les nouveau-nés. Chez l'homme, les effets cliniques de l'intoxication mercurielle constituent l'hydrargyrisme.
GÉOGRAPHIE
La production mondiale avoisine 3 000 t. L'Espagne est le premier producteur mondial (environ 1 500 t), devant la Chine (600 t), l'ex-U.R.S.S. (450 t) et l'Algérie (250 t).
PHARMACIE
Employé en thérapeutique depuis l'Antiquité, le mercure a perdu de son intérêt au profit d'autres médicaments plus actifs et moins toxiques. Restent encore employés le bichlorure (sublimé) comme antiseptique, le protochlorure (calomel) comme cholagogue et purgatif, les oxydes, jaune et rouge, en pommades dermatologique et ophtalmologique. Le cyanure de mercure est utilisé dans certains cas de syphilis viscérale, les diurétiques mercuriels sont pratiquement abandonnés. On emploie pour la désinfection des plaies la mercurescéine et le mercurobutol.




