diagramme (suite)
À un même phénomène peuvent correspondre, pour un système, suivant les grandeurs choisies, plusieurs diagrammes, parmi lesquels certains sont, en raison de propriétés qui leur sont attachées, plus utilisés ; c’est ainsi qu’en thermodynamique les transformations subies par un gaz sont utilement représentées dans le repère orthonormé où le volume v du gaz est porté en abscisse et sa pression p en ordonnée (repère dit « de Clapeyron »). Le diagramme obtenu possède une propriété importante : le travail effectué par les forces de pression du gaz durant la transformation,  est proportionnel à l’aire de la portion de plan comprise entre la courbe du diagramme (fig. 1a), l’axe des abscisses et les deux droites v = v1 et v = v2 ; si la transformation est fermée, c’est-à-dire si l’état final du gaz est identique à son état initial (v. cycle), le diagramme de Clapeyron est une courbe fermée (fig. 1b), et le travail des forces de pression,
est proportionnel à l’aire de la portion de plan comprise entre la courbe du diagramme (fig. 1a), l’axe des abscisses et les deux droites v = v1 et v = v2 ; si la transformation est fermée, c’est-à-dire si l’état final du gaz est identique à son état initial (v. cycle), le diagramme de Clapeyron est une courbe fermée (fig. 1b), et le travail des forces de pression, 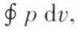 est proportionnel à l’aire intérieure à cette courbe fermée. Un autre diagramme, dit « entropique », où l’entropie du gaz est portée en abscisse et sa température en ordonnée, possède, relativement, cette fois, à la chaleur échangée, une propriété analogue à la précédente.
est proportionnel à l’aire intérieure à cette courbe fermée. Un autre diagramme, dit « entropique », où l’entropie du gaz est portée en abscisse et sa température en ordonnée, possède, relativement, cette fois, à la chaleur échangée, une propriété analogue à la précédente.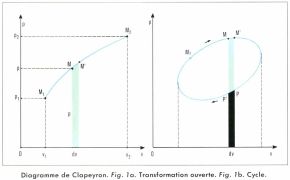
L’ensemble des équilibres thermodynamiques d’un corps pur ou d’un système de corps purs peut être clairement représenté par des diagrammes ; dans le cas d’un seul corps pur, la variance des équilibres étant au maximum égale à deux, on peut représenter sur un diagramme plan l’ensemble de ces équilibres ; le diagramme température-pression est particulièrement suggestif, car l’ensemble des états diphasés du corps pur s’y place sur trois courbes de forme caractéristique (v. corps pur). Pour les mélanges de deux corps purs, la variance maximale est de trois, et la représentation complète des équilibres nécessiterait un diagramme à trois dimensions : température, pression, proportions. Il est plus commode de ramener à deux le nombre des variables en fixant la valeur de l’une d’elles ; on obtiendra par exemple un diagramme isobare en fixant la valeur de la pression ; c’est ainsi qu’on figure ordinairement, dans le repère titres-températures, le diagramme d’ébullition d’un mélange homogène de deux liquides ou les diagrammes de cristallisation de mélanges et d’alliages binaires. Le cas des mélanges ternaires (par exemple alliages Pb, Sn, Bi) est encore plus compliqué, car les variables indépendantes sont au nombre de quatre. On fixe l’une d’entre elles, par exemple la pression, ce qui ramène au cas précédent d’un diagramme à trois dimensions : température et deux titres (la somme des trois titres est égale à 1). On porte la température verticalement et l’on fait usage, dans le plan horizontal, d’une base triangulaire équilatérale (fig. 2) : un mélange homogène de titres Ma, Mb, Mc, des trois corps Pb, Sn, Bi (Ma + Mb + Mc = 1 = la hauteur du triangle), est représenté, aux diverses températures, par la verticale du point M ; on peut donc traduire en un diagramme trilinéaire (ou ternaire), à l’intérieur du triangle, l’évolution isotherme de l’équilibre du système des trois corps en fonction de sa composition.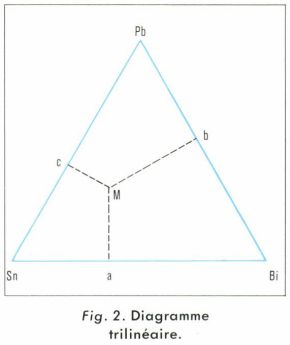
R. D.
G. Gourdet et A. Proust, les Diagrammes thermodynamiques (Dunod, 1950 ; 2 vol.).




