ion (suite)
Les ions en physiologie et en médecine
Dans les milieux organiques, la présence des ions minéraux et des substances non ionisées est étroitement liée au métabolisme de l’eau et au maintien de l’équilibre acido-basique*. Les principaux ions intéressant la biochimie clinique sont, pour les anions, les halogènes* : le fluor F–, le chlore Cl–, le brome Br–, l’iode I–, le fer Fe– –, le calcium* Ca– –, le magnésium Mg– et principalement le potassium K– et le sodium Na– ; pour les cations, les acides sulfuriques SO3+, phosphorique PO4+, et principalement le chlore Cl+ et l’acide carbonique CO3H+. Les électrolytes les plus abondants sont, de loin, le chlore, l’acide carbonique, le potassium et le sodium, dont la mesure, avec celle des protides qui jouent un rôle tampon, est pratiquement suffisante pour l’établissement de l’ionogramme ou dosage des ions d’un liquide.
La concentration d’un liquide en substances dissociées ou non détermine sa pression osmotique, qu’on évalue en milliosmoles, l’osmole étant par définition la pression osmotique conférée à 1 litre d’eau, à 0 °C et 760 mm de mercure, par une molécule non dissociée, soit 22,4 atmosphères. Pratiquement, on substitue au milliosmole le milliéquivalent (mEq), calculé en divisant la concentration en mg/1 par la valence-gramme. Cette valence étant le plus souvent égale à 1, la notation en mEq rend compte clairement de l’équilibre anion-cation.
La pression osmotique est due non seulement aux électrolytes, mais aussi aux protéines et aux substances organiques telles que l’urée ou le glucose, qui sont présents dans le plasma à des doses relativement élevées, ce dont il faut tenir compte dans les méthodes de mesures globales telles que la cryoscopie (abaissement du point de congélation), la mesure de la résistivité, l’adsorption sur résines catio-anioniques.
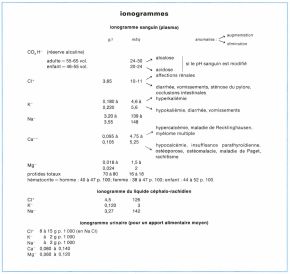
Détermination de l’ionogramme
• Ion CO3H+. Cet ion constitue la majeure partie des réserves de bases (bicarbonates alcalins) susceptibles de neutraliser les acides introduits par les métabolismes, dans le dessein de maintenir constant le pH sanguin. La réserve alcaline se dose par acidimétrie ou par volumétrie ; on a coutume de l’exprimer en « volumes » de gaz carbonique libérable de 100 ml de plasma.
• Ion Cl+. Le chlore est plus abondant dans le plasma que dans les globules, le rapport érythroplasmatique (chlore globulaire/chlore plasmatique) étant normalement égal à 0,50. On dose le chlore par les méthodes chimiques classiques : argentimétrie ou mercurimétrie.
• Ions K– et Na–. Classiquement, l’ion potassium est l’ion des cellules, l’ion sodium étant celui des liquides interstitiels, la perméabilité des membranes étant beaucoup plus rapide pouf le potassium que pour le sodium. Les méthodes de dosage du potassium à l’état de cobaltinitre et du sodium à l’état d’acétate triple d’uranyle, de magnésium et de sodium, méthodes chimiques précises, mais longues et délicates, ont cède la place aux méthodes physiques de photométrie de flamme, beaucoup plus rapides et permettant l’exécution d’examens demandés d’urgence. Outre leur rôle dans l’équilibre des liquides, les ions potassium et sodium interviennent dans la transmission de l’influx nerveux. L’ionogramme peut comporter le dosage des ions calcium Ca– – et magnésium Mg– . il comporte obligatoirement le dosage des protides totaux et la détermination de l’hématocrite (rapport volume globulaire/volume sanguin).
R. D.
R. Audubert, les Ions en solution (P. U. F., 1955 ; 2 vol.). / J. L. Delcroix, Introduction à la théorie des gaz ionisés (Dunod, 1958).




