corps pur (suite)
Les isothermes dont la température est comprise entre – 56,6 °C et + 31 °C possèdent un palier de liquéfaction, portion rectiligne parallèle à Ov ; la longueur de ce palier décroît quand la température s’élève, et s’annule à 31 °C ; la courbe de saturation, lieu des extrémités de ces paliers, est formée de deux parties : abrupte du côté liquide, c’est la courbe d’ébullition ; peu inclinée du côté gaz, c’est la courbe de rosée ; ces deux parties se raccordent en un maximum pour la température de 31 °C, température critique du CO2. L’isotherme critique, dont le palier de liquéfaction est de longueur nulle, présente, au sommet de la courbe de saturation, un point d’inflexion à tangente horizontale ; c’est le point critique C, figuratif d’un état remarquable du fluide pour lequel toutes les propriétés et les constantes physiques de la vapeur saturante se confondent avec celles du liquide.
La température de – 56,6 °C est celle du point triple de CO2 ; à cette température, les trois phases, solide, liquide, vapeur, peuvent coexister ; la pression d’équilibre est elle-même déterminée, car cet équilibre est invariant ; elle est de 5,1 atmosphères pour CO2.

Surface caractéristique du corps pur
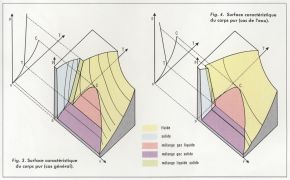
À chaque température, et pour une masse donnée du corps pur, il existe une relation entre sa pression p et son volume v ; il revient au même de dire que tous les états d’une masse donnée du corps pur satisfont à une relation f(p,v,T) = 0, que l’on peut, dans le repère d’axes Ov, OT, Op, représenter par une surface, la surface caractéristique du corps pur. Elle a la même allure pour un grand nombre de corps purs, CO2 par exemple ; la figure 3 en représente une partie, limitée par les plans de coordonnées et par des plans parallèles à ceux-ci. On retrouve les isothermes en coupant la surface par des plans T = constante, mais on peut aussi, en coupant par des plans v = constante, obtenir les isochores, et, par des plans p = constante, les isobares de changement d’état. La surface présente trois portions cylindriques de génératrices parallèles à Ov et qui se projettent sur le plan TOp suivant les courbes de vaporisation, de fusion, de sublimation du corps pur, et dont le point commun est le point triple.
Le reste de la surface est constitué par deux plages correspondant aux états monophasés du corps pur : l’état solide (cristallisé) et l’état fluide ; on ne peut passer de l’une à l’autre sans franchir une portion cylindrique, c’est-à-dire sans passer par un état diphasé : il y a une discontinuité essentielle entre les états solide cristallisé et fluide, c’est-à-dire entre Tordre et le désordre. Par contre, on peut aller d’un point à l’autre de la plage fluide sans pénétrer dans une zone d’états diphasés, c’est-à-dire sans observer de discontinuité dans les propriétés ; le passage de la vapeur sèche au liquide, qui est marqué d’une discontinuité caractérisée par la coexistence de deux phases de propriétés différentes si l’on pénètre dans le domaine des états diphasés, s’effectue au contraire par une variation continue des propriétés d’une masse constamment homogène si le chemin suivi sur la surface « contourne » le point critique.
La surface de la figure 3 correspond au cas le plus général, celui des corps qui augmentent de volume en fondant. Pour quelques corps cependant (l’eau, le bismuth, le gallium), il y a diminution de volume lors de la fusion ; corrélativement, la courbe de fusion est à pente négative ; cela entraîne un changement dans l’aspect de la surface caractéristique (fig. 4).
Thomas Andrews
Physicien irlandais (Belfast 1813 - id. 1885). Étudiant en 1869 la compressibilité du gaz carbonique, il a découvert le point critique et observé la continuité des états liquide et gazeux.
R. D.




