chlorures d’acides carboxyliques (suite)
Préparations
Pratiquement, toutes les préparations font appel à l’acide carboxylique ou à un de ses sels alcalins.
Les chlorures d’acides minéraux (ou assimilés) transforment les acides en chlorures d’acides :
R—COOH + PCl5 → OPCl3 + HCl + R—COCl,
R—COOH + SOCl2 → SO2 + HCl + R—COCl,
R—COOH + COCl2 → CO2 + HCl + R—COCl.
OPCl3 transforme les sels alcalins, pris sans excès, en chlorures d’acides :
3 RCO2Na + OPCl3 → OPO3Na3 + 3 R—COCl.
Les chlorures d’acides sont nettement plus volatils que les acides correspondants. Miscibles aux hydrocarbures, ils agissent assez vite sur les fonctions hydroxylées et aminogénées pour que leur solubilité dans l’eau, les alcools, les aminés n’ait guère de sens.
Propriétés chimiques
Réductions
Les chlorures d’acides sont réduits catalytiquement (Pt, Pd) en deux phases :
R—COCl + H2 → HCl + R—CHO ;
R—CHO + H2 → R—CH2OH.
L’arrêt à l’aldéhyde exige l’emploi d’un catalyseur désactivé par chauffage sur support de sulfate de baryum ou par empoisonnement partiel.
Les métaux sembleraient devoir conduire à une réduction duplicative :
2 R—COCl + 2 Na → 2 NaCl + R—CO—CO—R,
mais la dicétone-α est réduite en ion ène-diolate  qui agit sur deux nouvelles molécules de chlorure d’acide ; d’où le diester d’ènediol
qui agit sur deux nouvelles molécules de chlorure d’acide ; d’où le diester d’ènediol
Action des composés à hydrogène mobile
Le schéma est en général le suivant :
R—COCl + Hρ → HCl + R—CO—ρ.
• Hydracides. L’équilibre
R—COCl + HI ⇌ HCl + R—COI
est très favorable au second membre.
• Eau. L’hydrolyse est instantanée pour les premiers termes et plus lente pour le chlorure de benzoyle :
R—COCl + H2O → R—COOH + HCl.
• Alcools et phénols. L’alcool R′OH (ou le phénol ΦOH) conduit vraisemblablement à un intermédiaire :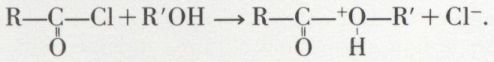
Si l’alcool est primaire ou s’il s’agit d’un phénol, ce complexe perd un proton ; d’où la formation de l’ester R—COOR′ ou R—COOΦ.
Mais, s’il est tertiaire, le complexe perd le radical R+ ; d’où le schéma global suivant :
R—COCl + (R′)3COH → R—COOH + (R′)3CCl.
On évite partiellement la seconde évolution en opérant en présence d’une base tertiaire (acylation pyridinée, meilleure préparation des esters).
• Aminés non tertiaires. Elles conduisent à des amides :
R—COCl + 2 HN(R′)2 → (R′)2NH2, Cl– + R—CO—N(R′)2.
• Hydrogène lié au carbone. En présence de chlorure d’aluminium, le benzène est acylé :
mais, sans catalyseur, les composés comprenant le groupe —CH2— lié à deux accepteurs sont acylés :
Actions des dérivés métalliques
• Les sels haloïdes lourds (KBr, RI) conduisent à un nouvel halogénure d’acide :
CH3—COCl + KI → KCl + CH3—COI (iodure d’acide).
• Les alcoolates, même tertiaires, engendrent des esters :
R—COCl + R′O– → Cl– + R—COOR′.
• Les sels d’acides conduisent à des anhydrides :
CH3—COCl + CH3—CO2Na → NaCl + CH3—CO—O—CO—CH3.
• Les organométalliques agissent de deux façons :
On s’arrête assez facilement à la première réaction si R′M est un organocadmien R′—CdCl, plus difficilement si c’est un acétylénique sodé R—C ≡ CNa, plus difficilement encore si c’est un organomagnésien R′MgX.
Propriétés de l’hydrogène en α
• Les chlorures d’acides  sont, à chaud, en présence d’une aminé tertiaire qui leur enlève HCl, transformés en le cétène (R)2C = C = O, qui, généralement, se polymérise.
sont, à chaud, en présence d’une aminé tertiaire qui leur enlève HCl, transformés en le cétène (R)2C = C = O, qui, généralement, se polymérise.
• En présence de chlorure d’aluminium, CH3—COCl se condense à lui-même :
C. P.




