savon
(latin sapo, -onis)

Produit obtenu par l'action d'un alcali sur un corps gras, et servant au nettoyage, ainsi qu'au blanchissage.
Caractéristiques et fabrication
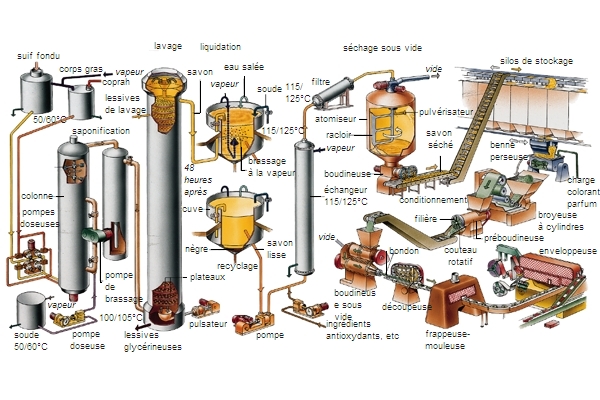
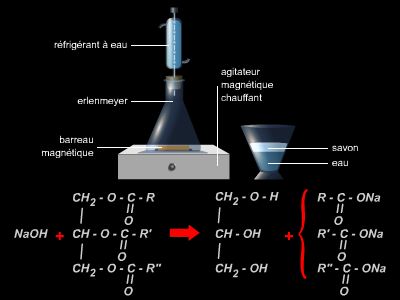
Le savon d'usage courant est essentiellement un mélange de sels de sodium d'acides gras provenant de corps gras : suif, arachide, palme, coco, olive, etc. La fabrication classique proprement dite selon le procédé « marseillais » comprend les étapes suivantes : saponification (réaction avec de la soude), cuisson (parachèvement de la saponification), lavages (séparation du glycérol et purification du savon), liquidation (mise en forme du savon pour utilisation ultérieure). La dernière phase, appelée finition, comprend les opérations de séchage, malaxage, boudinage, coupage, estampage et, enfin, emballage. Au cours du malaxage sont ajoutés un certain nombre d'ingrédients qui donnent ses caractéristiques au produit : talc, charges, colorants, parfums, séquestrants, déodorants.
Comment le savon lave-t-il ?
Le savon est un produit tensioactif : il abaisse la tension superficielle de l'eau et lui permet ainsi de mieux s'étaler sur une surface ; autrement dit, il améliore son pouvoir mouillant. Par ailleurs, les molécules de savon se présentent sous la forme de longues chaînes d'atomes. Elles comportent une « tête » hydrophile (qui peut se lier à l'eau), porteuse d'une charge électrique négative, et une longue « queue » hydrophobe (insoluble dans l'eau) mais qui a de l'affinité pour les graisses. Dans l'eau, elles ont ainsi un comportement bien particulier. Lors du lavage, elles se regroupent en structures sphériques, les micelles, autour des salissures grasses auxquelles elles se fixent par leur queue hydrophobe. Le mélange salissures/savon est finalement éliminé avec l'eau de rinçage.
Lors de la toilette, le savon dissout la graisse qui recouvre la peau et l'entraîne dans l'eau avec les saletés qu'elle contient. Mais le savonnage – ou tout lavage à l'aide de produits comportant des tensioactifs, par exemple les gels pour la douche ou les lessives – a pour inconvénient de fragiliser momentanément la peau en éliminant le film protecteur gras naturel qui la recouvre.
Pourquoi le savon mousse-t-il ?
La mousse de savon se forme lorsque des molécules de savon s'accolent les unes aux autres dans l'eau, du fait de leur structure très particulière (une extrémité hydrophile, l'autre hydrophobe).
Si l'on agite de l'eau propre, en l'absence de savon, on voit des bulles d'air remonter à la surface et éclater presque aussi vite qu'elles sont apparues. Si l'on agite de l'eau savonneuse, les molécules de savon se regroupent et emprisonnent une fine couche d'eau pour fabriquer la paroi d'une bulle de savon. Les bulles d'air sont alors « encapsulées » dans cette paroi qui les empêche d'éclater quand elles remontent à la surface.







