quantiques (nombres) (suite)
Les valeurs possibles de l, correspondant à une valeur de n donnée, sont tous les nombres entiers obéissant aux inégalités :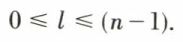
m est le nombre quantique magnétique orbital, tel que nous l’avons défini plus haut. Ses valeurs possibles, correspondant à une valeur donnée de l, sont tous les nombres entiers qui obéissent aux inégalités : 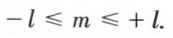 Ce nombre m représente en quelque sorte l’orientation dans l’espace du vecteur moment cinétique orbital ; on le désigne souvent avec la notation plus précise ml.
Ce nombre m représente en quelque sorte l’orientation dans l’espace du vecteur moment cinétique orbital ; on le désigne souvent avec la notation plus précise ml.
Les fonctions d’onde Ψnlm correspondant à la même valeur de n, mais à des valeurs distinctes de l et m, représentent des états différents de l’atome, bien que ceux-ci correspondent à la même valeur de l’énergie E.
Les fonctions d’onde Ψnlm ne suffisent pas à représenter complètement les états de l’atome d’hydrogène. Il faut encore tenir compte du moment cinétique de spin de l’électron : à celui-ci correspond un nombre quantique magnétique de spin que l’on désigne par ms et qui peut prendre les deux valeurs 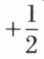 et
et 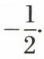
La théorie des autres atomes, à plusieurs électrons, est bâtie en généralisant les calculs relatifs à l’atome d’hydrogène. On montre que chaque électron peut être caractérisé par quatre nombres quantiques n, l, ml, ms ayant la même signification que ci-dessus. L’énergie de liaison dépend principalement de n, mais peut aussi dépendre de l. On aboutit ainsi à la notion de couches et sous-couches électroniques, qui sont désignées par des lettres correspondant aux diverses valeurs des nombres quantiques n et l, conformément au tableau ci-dessous :
La clef de la structure électronique de l’atome est alors fournie par le principe de Pauli : il ne peut pas y avoir dans le même atome deux ou plusieurs électrons caractérisés par quatre nombres quantiques identiques ; les électrons diffèrent toujours les uns des autres par l’un au moins de ces quatre nombres. Cela permet d’expliquer théoriquement la classification des atomes édifiée par D. I. Mendeleïev à partir de leurs propriétés chimiques.
Deux savants
Samuel Abraham Goudsmit (La Haye 1902) et George Eugène Uhlenbeck (Batavia [auj. Djakarta] 1900), physiciens américains d’origine hollandaise. Ils créèrent en 1925 la théorie du spin de l’électron et attribuèrent à celui-ci un moment magnétique.
B. C.




