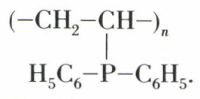polymère pétrochimique (suite)
Le polystyrène (C6H5CHCH2)n
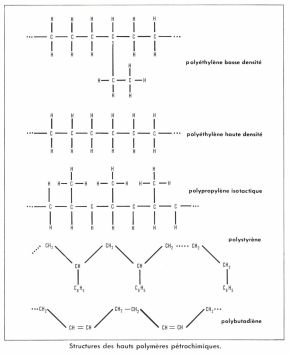
Sa molécule peut être considérée comme celle d’un polyéthylène linéaire, mais avec un noyau benzénique fixé à un atome de carbone sur deux de la chaîne droite. Le polystyrène est un thermoplastique qui ne cristallise pas, mais se solidifie en un produit vitreux se ramollissant vers 80 °C, transparent, teinté ou opaque.
Le styrène, hydrocarbure monomère, est synthétisé à partir du benzène, lui-même extrait des essences aromatiques obtenues dans les raffineries de pétrole par reforming ou par steam-cracking.
Le polystyrène peut être coulé, moulé ou laminé très facilement pour donner des objets ménagers de grande consommation : jouets, accessoires électriques, équipement interne de réfrigérateurs ; c’est en particulier un excellent isolant. Par insufflation de minuscules bulles d’air, on fabrique le polystyrène expansé, mousse solide blanche très légère, d’un emploi universel comme calorifuge, frigorifuge et qui remplace la paille pour l’emballage d’objets fragiles.
Les polydioléfines
Le caoutchouc naturel est le prototype de ces hauts polymères, appelés aussi polydiènes, dont le monomère est une « diène », ou dioléfine, hydrocarbure comportant deux doubles liaisons : il est, en effet, le polymère d’un isoprène CH2=C(CH3)—CH=CH2. L’industrie des élastomères, ou caoutchoucs synthétiques, copie donc la nature en polymérisant des dioléfines.
Le polyisoprène de synthèse a des propriétés semblables à la gomme naturelle, mais sa fabrication est limitée par le coût relativement élevé de l’isoprène pétrochimique, tiré de l’essence de steam-cracking.
Le polybutadiène, très semblable au précédent et voisin du produit naturel, s’obtient à un moindre prix de revient à partir du butadiène CH2=CH—CH=CH2, présent en abondance dans les gaz liquéfiés issus du steam-cracking.
La copolymérisation du styrène et du butadiène donne le caoutchouc* synthétique courant (SBR ou BUNA), tandis que celle de l’isobutène (CH3)2C=CH2 et de l’isoprène donne le caoutchouc butyle.
Procédés de polymérisation
L’assemblage de ces centaines ou de ces milliers de molécules se fait à l’état liquide, ce qui suppose la liquéfaction préalable des hydrocarbures normalement gazeux, comme l’éthylène, le propylène ou le butadiène, sous l’action de la chaleur et d’un ou de plusieurs catalyseurs, substances comportant des ions métalliques qui provoquent l’ouverture des doubles liaisons et entraînent le phénomène de polymérisation. Une fois en cours, celle-ci dégage de la chaleur qu’il faut dissiper en remuant et en refroidissant le mélange sous peine de surchauffe et de décomposition. Lorsque le polymère est parfaitement soluble dans le monomère, comme c’est le cas pour le polystyrène, l’ensemble forme une phase sirupeuse, puis progressivement pâteuse, et, en réglant la température, il est possible d’obtenir au fond de l’appareil le produit fini et de l’en extraire, à l’aide d’une pompe à vis, à l’état liquide. Le produit est ensuite étiré en « spaghetti », refroidi par immersion dans un bain d’eau et coupé en pastilles.
Généralement, le polymère est peu soluble, ou même insoluble, dans le monomère, l’ensemble formant une boue impossible à pomper ou à agiter. L’adjonction d’un solvant capable de dissoudre l’un et l’autre produit permet de surmonter cette difficulté : c’est ainsi que le polyéthylène s’obtient par polymérisation sous pression, en solution dans une essence spéciale, comme du cyclohexane, solvant qui est ensuite éliminé à l’eau bouillante ; le polymère est précipité, puis séché à l’air chaud dans un four rotatif avant d’être tréfilé par extrusion. Le polypropylène et le polyisobutène sont également fabriqués par des procédés avec solvant.
Dans la polymérisation par émulsion, le ou les monomères sont d’abord mélangés à de l’eau contenant un agent émulsificateur, comme un savon, pour former une suspension laiteuse de particules stables. Au cours de la réaction, il se forme un latex, qui est une émulsion du polymère. Les élastomères sont souvent obtenus par cette méthode.
A.-H. S.
➙ Aromatiques (hydrocarbures) / Éthylène / Pétrochimie / Polymérisation / Propylène / Steam-cracking.