état
(latin status, de stare, se tenir)

Nature sous laquelle se présente un corps.
PHYSIQUE
Introduction
La matière est le premier concept physique, le plus concret, et apparemment le plus simple. Pourtant, au-delà de cette apparence, les hommes se sont toujours interrogés sur la nature de la matière, et les théories les plus évoluées n'ont fait que renforcer son caractère étrange.
Parmi les descriptions de la matière, la théorie quantique est, dans l'état actuel des connaissances, l'outil le plus rigoureux pour décrire les propriétés physiques et chimiques de la matière. Elle bouleverse cependant les images intuitives à travers lesquelles nous percevons la matière. Il n'est heureusement pas nécessaire de réconcilier l'intuition avec la théorie quantique pour parvenir à décrire les différents états de la matière.
En effet, si le formalisme quantique est indispensable pour rendre compte de la structure interne des atomes, une description très simple des atomes suffit en général pour représenter les états de la matière. Ces derniers sont déterminés par deux types de propriétés : la nature des états de liaison entre les atomes constituant le matériau considéré, et le type et le degré d'organisation spatiale et temporelle des atomes entre eux.
De la notion au concept
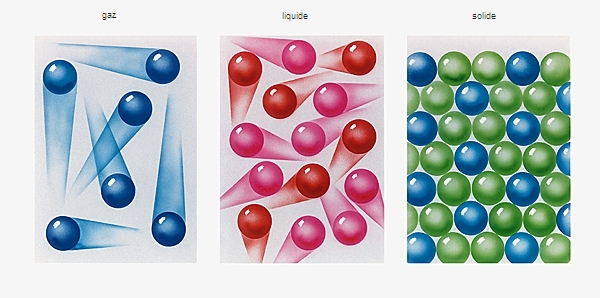
Historiquement, les Grecs furent les premiers à tenter une classification de la multitude des objets matériels qui se présentaient à eux. Ils fondèrent cette classification sur les états dans lesquels apparaît la matière (solide, liquide, gazeux) et sur certaines de ses propriétés. Pour Aristote, il existait quatre éléments essentiels : la terre, l'eau, l'air et le feu. Les Grecs se sont interrogés également sur la nature de la matière. Est-elle indéfiniment sécable en parties qui conservent les mêmes propriétés ? Ou bien est-elle constituée de petits grains insécables, littéralement des « atomes » ? Démocrited'Abdère défendra, quatre siècles avant notre ère, l'image d'une matière constituée d'atomes en mouvement : selon lui, la diversité des états et des formes de la matière est simplement due à la multiplicité des combinaisons possibles de position et de mouvement de ces atomes, particules matérielles immuables et indivisibles. Cette image mécaniste du monde – selon laquelle la matière a des propriétés essentiellement géométriques et mécaniques – marquera en profondeur les sciences physiques aux xixe et xxe s.
Aristote avait proposé une autre description de la matière, dans laquelle priment les formes qui lui sont conférées… par la nature, par Dieu, ou par l'homme : une table est, par exemple, de la matière bois, sculptée ; si l'on s'intéresse au bois, il est constitué de matière cellulaire agencée sous forme de fibres agrégées, plus ou moins desséchées, etc. La notion de matière recule ainsi à l'infini, tel un ultime noyau caché à l'intérieur de formes qui s'emboîteraient indéfiniment les unes dans les autres, comme des poupées russes.
La genèse de la classification périodique
L'influence de la conception aristotélicienne de la matière va perdurer pendant deux millénaires. Cependant, les alchimistes essaieront de découvrir la matière fondamentale, celle qui serait à l'origine de tout : ils réalisent ainsi les premiers essais d'analyse et de synthèse, et certaines propriétés chimiques et physiques de différents corps sont découvertes et classées.
Les savants du xviie et du xviiie s. reprennent cet héritage, en introduisant de nouvelles méthodes de travail ; ils entreprennent une étude systématique des propriétés chimiques des différents corps, qui conduit à la notion d'élément chimique.
Antoine Laurent de Lavoisier, par exemple, montre que l'eau est composée de deux éléments, l'hydrogène et l'oxygène, impossibles à obtenir eux-mêmes par une combinaison d'autres éléments : ce sont des éléments de base. Quelques dizaines d'éléments sont ainsi identifiés, dont les propriétés chimiques peuvent être classées par référence à leur affinité pour l'oxygène : éléments oxydables, éléments oxydants.
Dimitri Ivanovitch Mendeleïev propose, en 1869, une classification systématique des éléments qui repose sur une périodicité approximative de l'affinité de certains éléments pour l'oxygène en fonction de leur masse. Le succès de cette classification est immense, car elle prévoit l'existence d'éléments, alors inconnus, de masse déterminée et devant présenter un type précis de propriétés chimiques ; ces éléments sont découverts quelques années plus tard, avec les propriétés prévues par cette classification ! Le tableau de Mendeleïev est ensuite interprété comme le reflet de la structure électronique de chaque élément : passer d'un élément à l'élément suivant signifie ajouter un électron à l'atome.
La description quantique
En 1897, sir Joseph John Thomson découvre l'électron, et Ernest Rutherford démontre en 1907 qu'un atome est constitué d'un noyau qui contient deux types de particules, les neutrons – sans charge électrique – et les protons – porteurs d'une charge opposée à celle de l'électron. Ensuite, les travaux d'Einstein sur l'émission photoélectrique et ceux de Max Planck sur le rayonnement du corps noir mettent en évidence les propriétés quantiques, c'est-à-dire particulaires, de la lumière. C'est une première grande brèche dans la physique classique, qui repose notamment sur l'image ondulatoire de la lumière, description bien assise grâce au formalisme des équations de James Clerk Maxwell.
Les physiciens découvrent que la lumière peut se comporter, suivant la situation expérimentale, soit comme une onde, soit comme un ensemble de particules. En 1927, Clinton J. Davisson et Lester H. Germer démontrent expérimentalement l'existence d'interférences dans un faisceau d'électrons réfléchi par un cristal de nickel : le comportement ondulatoire des électrons est établi sans ambiguïté, la matière – comme la lumière – se révèle tantôt particulaire, tantôt ondulatoire, suivant la situation expérimentale. Depuis, des progrès considérables ont été effectués dans la compréhension de la structure de la matière à l'échelle infra-atomique, par exemple par l'introduction des quarks, particules fondamentales constitutives du proton et du neutron. Cependant, la description des propriétés « courantes » de la matière (mécaniques, optiques, électriques…) repose sur les propriétés du cortège électronique de l'atome, elles-mêmes établies par la théorie quantique au cours du premier quart du xxe s.
La thermodynamique : « deus ex machina »
Parallèlement à ce travail sur les propriétés chimiques des éléments débutent, au cours du xixe s., des études approfondies sur les états de la matière. L'état gazeux est particulièrement bien compris, car il est le plus simple ; il devient le fondement de la science thermodynamique, qui décrit les échanges énergétiques au sein de la matière. Les travaux de Sadi Carnot, puis ceux de Ludwig Boltzmann posent les bases théoriques de la thermodynamique, et permettent ainsi de décrire les changements d'état de la matière. Au xxe s., les contributions des physiciens Lev D. Landau, Ilya Prigogine et Kenneth Wilson affinent considérablement la description des changements d'état de la matière, nommés également transitions de phase. La vision d'Aristote d'une matière informe sculptée par la nature est ainsi relayée par le deuxième principe de la thermodynamique. Selon les physiciens, le premier des mécanismes qui sculptent la matière est la tendance de l'Univers à augmenter son désordre : son entropie.
Les outils de description
La théorie quantique est le premier outil de description de la matière ; très puissant, cet outil exige cependant l'utilisation d'un formalisme pesant. Il permet un calcul rigoureux des états fondamentaux, c'est-à-dire des états au repos de systèmes microscopiques – ne comportant que quelques atomes, voire quelques dizaines d'atomes –, mais au prix d'un travail laborieux sur des ordinateurs puissants. Une telle description est rapidement impraticable si l'on s'intéresse à l'évolution de ces systèmes dans le temps et dans l'espace sous l'effet d'un apport d'énergie lumineuse, électrique, mécanique, magnétique ou chimique. Il est actuellement impensable d'effectuer le calcul rigoureux de l'état de systèmes contenant une quantité d'atomes de l'ordre du nombre d'Avogadro, c'est-à-dire de taille macroscopique, de l'ordre du centimètre cube, à partir de la théorie quantique. Fort heureusement, les résultats décisifs peuvent le plus souvent être caractérisés principalement par quelques types de liaisons interatomiques : il est alors possible d'appliquer une description classique à l'ensemble des atomes, reliés entre eux par des « liaisons » que caractérisent quelques propriétés simples.
Les différents types de liaisons chimiques
Deux atomes qui s’attirent peuvent former une liaison chimique : ils gagnent, à être proches l'un de l'autre, une quantité d'énergie potentielle. On distingue ainsi les liaisons fortes, dont l'énergie associée est de l'ordre de 1 eV ou supérieure. Dans ce cas, la paire d'atomes en interaction fait apparaître des états électroniques complètement nouveaux pour les électrons ; ainsi, dans les liaisons ioniques, un ou plusieurs électrons d'un atome sont cédés à l'autre atome. Ce type de liaison se rencontre, par exemple, dans des sels tels que le chlorure de sodium (NaCl). Un autre type de liaison forte caractéristique est la liaison covalente, dans laquelle des électrons isolés de chacun des atomes s'associent pour former des paires d'électrons fortement liées. Les liaisons covalentes, contrairement aux liaisons ioniques, sont en général anisotropes, c'est-à-dire qu'elles tendent à s'orienter dans des directions particulières de l'espace.
Par opposition, les liaisons d'énergie inférieure ou de l'ordre de 0,1 eV sont nommées liaisons faibles. Les états électroniques des atomes isolés sont peu modifiés par l'interaction. C'est le cas des forces d'attraction dites de Van der Waals, que l'on rencontre dans le processus d'adhérence des molécules en longues chaînes, les polymères, utilisés par exemple pour les rubans adhésifs.
L'organisation spatiale d'un grand nombre d'atomes : ordre et désordre
La taille du nombre d'Avogadro étant considérable, la matière semble continue à notre échelle : le déplacement d'un seul atome n'est pas perceptible. Mais elle peut prendre des formes et des textures très diverses, suivant son état ; elle peut aussi présenter des orientations préférentielles, parallèlement à une direction ou à une surface. Ces états sont généralement caractérisés par une (ou des) longueur(s) associée(s) à des propriétés bien précises.
L'utilisation des méthodes statistiques (emploi de la mécanique statistique, ou physique statistique), lorsqu'une multitude d'atomes sont mis en jeu dans une quantité macroscopique de matière, permet d'obtenir des résultats remarquables.
Cette approche de l'organisation spatiale des atomes rejoint les résultats de la thermodynamique, fondée sur les deux principes suivants : selon le premier, l'énergie de l'Univers peut changer de forme à condition de se conserver globalement ; selon le second, le désordre doit être maximal dans un système physique isolé. La thermodynamique est, en quelque sorte, une économie de l'énergie dans les systèmes physiques. Elle permet en principe de déterminer quels sont les états d'équilibre d'un système en postulant que le désordre de l'Univers entier (considéré comme un système isolé) est maximal : une quantité de matière isolée du reste de l'Univers tend ainsi vers un maximum d'entropie. Si l'on tient compte des échanges d'énergie, d'espace ou de matière avec le reste de l'Univers, la conséquence des principes de la thermodynamique est alors, en général, que le système étudié s'ordonne à basse température, et qu'il adopte un état désordonné à haute température. Ces transitions ordre/désordre apparaissent dans des systèmes physiques très variés.
L'organisation temporelle et les propriétés de transport
Les mouvements des atomes au sein de la matière peuvent être complètement désordonnés au niveau microscopique et ne correspondre à aucun mouvement à notre échelle. C'est le cas des mouvements des atomes ou des molécules dans un gaz ou dans un liquide, c'est aussi le cas des vibrations des atomes dans un solide, qui sont ordonnées à courte distance mais en général désordonnées à l'échelle macroscopique. La facilité, ou la difficulté, à faire circuler un courant électrique ou un flux de matière dépend fortement des caractéristiques de l'état dans lequel se trouve la matière. Le diamant et le graphite sont, par exemple, deux formes cristallines du carbone pur : le diamant est un très bon isolant électrique, tandis que le graphite est conducteur.
Les états structurés à courte distance
La notion d'ordre est le fil directeur de cette exploration des états de la matière. Certains états ne présentent cependant pas d'organisation régulière au-delà de l'échelle microscopique. Ce sont les états gazeux et liquide, que l'on regroupe sous le nom d'état fluide. C'est aussi le cas des solides désordonnés, dits solides amorphes. Enfin, dans l'état de plasma, où la température dépasse le million de degrés, la matière présente un comportement fort complexe.
Les fluides
Une propriété macroscopique simple caractérise l'état fluide : un fluide s'écoule et se déforme sous l'effet de forces très faibles. De façon plus précise, on dit que les fluides ne présentent pas de résistance au cisaillement.
À l'échelle microscopique, les fluides – à l'exception des cristaux liquides – ne sont pas organisés sur de grandes distances. L'agitation des atomes entraîne un brassage permanent de leurs positions. Deux états fluides qui nous sont familiers, le gaz et le liquide, se distinguent par des propriétés différentes : les gaz sont mille fois moins denses que les liquides, et sont compressibles alors que les liquides le sont très peu.
À l'échelle atomique, la différence est également remarquable. Les molécules d'un gaz ont peu d'interactions sur la plus grande partie de leur trajectoire (99,9 %), elles sont isolées dans le vide, et les collisions n'affectent que 0,1 % de celles-ci. Le désordre, c'est-à-dire l'entropie, associé à leur position est important. Les molécules d'un liquide sont, au contraire, en interaction permanente avec leurs voisines, et bénéficient ainsi de l'abaissement de leur énergie potentielle dû à l'attraction mutuelle. L'entropie associée au désordre de leur position est cependant plus faible que dans un gaz ; mais, à la température d'ébullition, les états gazeux et liquide d'un même corps coexistent en équilibre. Dans un gaz, l'énergie cinétique des molécules est élevée, et l'entropie (Sg) est également plus élevée que celle du liquide (Sl), car le désordre des positions y est plus grand. Dans un liquide, l'énergie totale des molécules est plus faible que dans un gaz, et ce en raison de l'énergie d'attraction gagnée et cédée au reste de l'Univers ; cette énergie cédée au reste de l'Univers en augmente l'entropie. L'état gazeux et l'état liquide contribuent donc tous deux à augmenter l'entropie de l'Univers. Dans les conditions de l'ébullition, le produit du gain d'entropie ΔS = Sg – Sl associé au désordre des positions atomiques par la température absolue T est juste équilibré par l'énergie potentielle liée à l'attraction mutuelle de ses molécules au sein du liquide. Ce produit L = T . ΔS est la chaleur latente qu'il faut fournir au liquide pour le vaporiser.
Au point critique, la matière hésite
L'un des résultats de la physique classique est que ΔS doit être supérieur à la constante de Boltzmann (k) pour que l'état gazeux et l'état liquide soient clairement différents. Pour un corps donné, il n'existe plus de frontière nette entre l'état liquide et l'état gazeux au-delà d'une température dite critique, telle que ΔS est de l'ordre de k. L'état du fluide hypercritique, lorsque ΔS est inférieur à k, est toujours homogène quelles que soient la pression et la densité : il n'y a plus ni gaz ni liquide mais un seul fluide qui n'est ni l'un ni l'autre.
Au point critique, c'est-à-dire au voisinage de la température critique et de la pression critique, les propriétés du fluide sont particulièrement intéressantes. En effet, le gain entropique dans le gaz équilibre exactement le gain d'énergie potentielle dans le liquide, comme au point d'ébullition, mais au point critique ces quantités sont également du même ordre que l'énergie caractéristique kT reçue de l'agitation thermique. Il en résulte un comportement d'« hésitation » de la matière entre l'état liquide et l'état gazeux, qui se traduit par l'apparition de régions très étendues de type liquide alternées avec des régions de type gaz. Ces régions, nommées fluctuations critiques, peuvent s'étendre sur plusieurs microns et produisent le phénomène bien visible et spectaculaire d'opalescence critique.
La notion de fluide est toute relative : à une échelle ou à une autre, la matière est toujours susceptible de s'écouler. Ainsi, à l'échelle de la Terre et des temps géologiques, une partie du manteau terrestre (l'asthénosphère), située entre 70 et 100 km de profondeur, se comporte comme un fluide. Ce niveau « plastique » permet à la croûte terrestre et à la partie du manteau située au-dessous (cet ensemble constitue la lithosphère), dont le comportement est plus rigide, de se déplacer par l'intermédiaire de plaques. La dérive des continents, qui renouvelle complètement la géographie continentale tous les 200 millions d'années, n'est ainsi que le fait de courants de convection dans le manteau terrestre.
Le gaz parfait, état de référence
L'état gazeux occupe une place particulière parmi les différents états de la matière en raison des faibles interactions de ses molécules. Les physiciens ont élaboré un modèle simplifié qui sert de référence, le gaz parfait. Ce modèle est très efficace, bien qu'il soit intrinsèquement contradictoire! Il suppose en effet que les atomes du gaz parfait présentent simultanément deux propriétés :
– ils n'interagissent pratiquement pas, au sens où leurs interactions représentent une énergie négligeable par rapport à leur énergie cinétique ;
– ils interagissent fortement, au sens où l'on peut considérer le gaz comme étant au point d'équilibre à chaque instant.
Moyennant cette « pirouette conceptuelle », ce modèle constitue la base de la description thermodynamique de tous les états de la matière où l'énergie associée aux interactions est faible. Dans de nombreuses situations – celles des gaz réels et des solutions diluées –, la matière se comporte presque comme le prévoit le modèle du gaz parfait.
Longueurs caractéristiques dans les fluides
Dans un assemblage désordonné d'atomes de diamètre a, deux distances caractéristiques sont importantes.
Tout d'abord la distance moyenne d entre les atomes. Il est relativement facile de la relier au nombre n de molécules par unité de volume en exprimant que chaque atome occupe en moyenne un volume d3. Une unité de volume est donc remplie par n petits volumes d3, soit n d3 = 1. La distance moyenne d varie ainsi comme la racine cubique de l'inverse de n.
Une seconde longueur, L, nommée libre parcours moyen, est la distance moyenne que parcourt un atome sans entrer en collision avec un autre atome. On schématise une collision par le fait que la distance entre les centres de deux atomes devient égale ou inférieure à 2a. Une telle collision se produit si, durant le mouvement d'un atome le long d'une direction, le centre d'un autre atome se trouve à l'intérieur du cylindre de rayon 2a axé selon cette direction. Dans un cylindre de longueur L, un seul centre d'atome est présent en moyenne. Le volume du cylindre est donc le volume moyen occupé par un atome : π (2a)2 . L = 1/n. La longueur L est donc inversement proportionnelle au nombre n d'atomes par unité de volume.
Dans un liquide, les atomes sont au contact les uns des autres dans un assemblage mouvant mais compact. Les trois longueurs a, d et L sont du même ordre, c'est-à-dire comprises entre 0,1 et 1 nm.
Dans un gaz à la pression atmosphérique, la masse volumique typique est de 1 kg/m3, soit mille fois moins que celle des liquides. Dans un liquide, le nombre d'atomes par centimètre cube est de l'ordre de 1022, tandis que dans un gaz il est de l'ordre de 10−9. La distance moyenne d entre deux atomes dans le gaz est typiquement de 3 nm, alors que le libre parcours moyen L est cent fois plus grand, soit environ 0,3 μm.
Les solides désordonnés à l'échelle atomique
Lorsqu'un fluide est suffisamment refroidi, il se condense sous forme solide. On connaît une seule exception à cette règle, l'hélium : il reste liquide même à très basse température. Suivant la vitesse de refroidissement, les atomes et molécules du liquide ont ou n'ont pas le temps de s'organiser au moment de la solidification. Si l'on opère très rapidement, le solide peut conserver un état désordonné, dit état amorphe, qui ressemble à un liquide figé. Cependant, certains mélanges d'atomes ne cristallisent pas, même s'ils sont refroidis lentement ; ils forment alors des verres, après être passés par un état pâteux lors du refroidissement. L'étude expérimentale et théorique des solides désordonnés est plus délicate que celle des solides cristallins. Le désordre apparent de ces structures cache en général une organisation plus fine et plus difficile à évaluer, qui entraîne des propriétés subtiles. Dans certaines régions volcaniques, on trouve des verres naturels (l'obsidienne), dont la formation est due à la trempe rapide d'un magma riche en silice arrivant en surface.
Un solide dans l'état amorphe présente des propriétés particulières, souvent bien différentes de celles du solide cristallin correspondant. La tenue mécanique d'un matériau amorphe est en général meilleure que celle des cristaux, et la conductivité électrique est bien différente. Ainsi, les propriétés supraconductrices du molybdène amorphe sont bien meilleures que celles du molybdène cristallin, ce qui signifie que le désordre dans la position des noyaux atomiques favorise, paradoxalement, l'apparition de l'ordre électronique lié à l'état supraconducteur. C'est un effet indirect de la suppression de l'ordre magnétique existant dans le molybdène cristallin, qui disparaît au profit de l'ordre supraconducteur dans le molybdène amorphe : l'état magnétique est plus stable que l'état supraconducteur, mais il est moins robuste face au désordre cristallin.
Une autre différence importante entre les solides cristallisés et les solides amorphes est la faible sensibilité de ces derniers aux impuretés et aux défauts. Le silicium utilisé pour réaliser les circuits électroniques des ordinateurs, par exemple, contient des impuretés volontairement ajoutées au cristal pour ajuster sa conductivité électrique : 1 atome de bore pour 100 millions d'atomes de silicium suffit à régler la conductivité du canal du transistor. En revanche, dans le silicium amorphe, il faut une proportion relativement importante d'impuretés pour modifier sensiblement la conductivité électrique. Cette propriété caractéristique des verres est exploitée lorsque l'on souhaite réaliser des composants électroniques d'une grande robustesse pouvant résister à un rayonnement ionisant.
Un état complexe : le plasma
Un plasma est un gaz d'atomes ou de molécules partiellement ou totalement ionisés. Des plasmas se produisent dans les étincelles ou dans les éclairs d'orage ; ils sont aussi la source de lumière dans les tubes au néon. En général, ils sont composés d'un mélange d'ions positifs et d'électrons, mais il existe aussi des plasmas d'ions négatifs. Les plasmas occupent une place d'exception dans les états de la matière : ils sont éloignés de l'équilibre thermodynamique, gardent longtemps la trace de leur états successifs et présentent des évolutions difficilement prévisibles. Leur comportement irrégulier et instable s'explique par les fortes interactions à longue distance des particules chargées.
Ce sont par ailleurs des états où la température de la matière peut dépasser plusieurs millions de degrés. Lorsque cette température est de l'ordre de 100 millions de degrés, l'état de plasma est sur le chemin de la fusion nucléaire. En effet, l'énergie cinétique des ions est suffisante pour que les noyaux interagissent fortement durant les collisions et induisent des réactions nucléaires, de fission ou de fusion. Si les gaz du plasma sont des atomes légers, il peut résulter de ces réactions que les noyaux produits par la fusion développent une grande énergie cinétique : ceux-ci peuvent alors échauffer le plasma, renforcer les réactions de fusion, et ainsi de suite. La réaction est alors divergente et peut produire une explosion : c'est le principe de la bombe H (à fusion d'hydrogène). Si cette réaction est contrôlée, la fusion nucléaire peut devenir une source d'énergie exploitable à grande échelle. Pour contrôler la production d'énergie, il faut connaître le comportement des plasmas à haute température et à forte densité. L'exploration de cet état de la matière depuis plus d’un demi-siècle a révélé une grande variété d'instabilités dans les plasmas à mesure que leur température augmente.
Il faut signaler l'étude récente des microplasmas constitués de quelques centaines à quelques milliers d'ions confinés par un champ électromagnétique. La température de tels plasmas peut être abaissée au voisinage du zéro absolu. Ces plasmas se comportent comme des solides ou comme des liquides, alors que la distance entre les ions est de plusieurs dizaines de microns, soit 100 000 fois plus que dans les solides ou liquides ordinaires. À la différence des plasmas, les microplasmas n'ont pour l'instant aucune autre application que l'étude de la matière.
Les états ordonnés à grande distance
Un solide est le plus souvent cristallisé, c'est-à-dire que ses atomes sont parfaitement rangés sur de grandes distances. Il n'y a pas de frontière nette entre ordre dit à courte distance et ordre dit à grande distance : l'un s'arrête à quelques distances atomiques, tandis que l'autre peut se propager sur des millions de distances atomiques. Selon la thermodynamique, le désordre tend à augmenter, et il semble étonnant que la matière s'ordonne spontanément dans certains cas. En fait, l'ordre, qui permet de diminuer l'énergie potentielle de la matière, s'installe à basse température, là où les bénéfices thermodynamiques de l'augmentation de l'entropie sont plus faibles. Les innombrables situations physiques où la matière s'ordonne sont définies par la géométrie de l'espace occupé par la matière et par le nombre de degrés de liberté de la quantité physique qui s'ordonne. Il est ainsi possible d'appliquer la même description, dite universelle, à des situations physiques aussi différentes que les aimants, les mélanges liquide-vapeur, les supraconducteurs ou les étoiles à neutrons.
Le magnétisme, un modèle pour la matière organisée
Les aimants, ou matériaux ferromagnétiques, perdent leur aimantation lorsqu'ils sont portés à une température supérieure à la température de Curie. Cette propriété, connue depuis la Renaissance, a été étudiée en détail par Pierre Curie dans sa thèse, en 1895. Dans la première moitié du xxe s., des physiciens comme Paul Langevin, Heike Kamerlingh Onnes, Pierre Weiss, Paul Ehrenfest, Louis Néel, Ernest Ising, Lars Onsager ou encore Lev Landau ont décrit les propriétés magnétiques de la matière afin de les relier à sa structure microscopique. Il s'agissait de décrire la façon dont l'aimantation varie en fonction de la température et du champ magnétique extérieur. L'étude de ces situations a débouché sur une description beaucoup plus générale des états ordonnés de la matière.
L'ordre spatial d'un ensemble d'objets microscopiques en interaction, selon Ernest Ising
Ernest Ising propose, en 1920, un modèle simple pour décrire les mécanismes microscopiques de l'aimantation d'un solide. Selon ce modèle, l'aimantation du solide est la somme vectorielle des aimantations locales dues aux spins des électrons. Les atomes constituant le solide sont situés aux nœuds d'un réseau cristallin de dimension d : sur une ligne d = 1, dans un plan d = 2, dans l'espace d = 3. Sur chacun des sites du réseau cristallin se trouve un spin qui se comporte comme un petit aimant, ou moment magnétique. Le calcul de l'aimantation est effectué dans le cadre de deux hypothèses.
Selon la première, les moments magnétiques sont tous identiques en module et s'orientent dans des directions cristallines privilégiées. Ising suppose que les moments magnétiques sont tous parallèles à une direction et que seul leur signe les différencie d'un site à l'autre, mais on peut aussi étudier les situations où les moments magnétiques ont des composantes dans deux ou trois directions. L'aimantation ou, plus généralement, une grandeur physique nommée paramètre d'ordre, qui permet de mesurer l'ordre, présente un nombre n de composantes (n = 1, 2 ou 3).
Selon la seconde hypothèse par le calcul de l'aimantation, deux moments magnétiques Si et Sj situés sur des sites voisins présentent une énergie d'interaction proportionnelle à leur produit Si . Sj. Il faut ensuite appliquer les principes de la thermodynamique pour calculer l'état d'équilibre d'un tel système en fonction de la température et du champ magnétique. On s'attend à ce que le diagramme de phase magnétique de ce système présente des propriétés universelles dépendant essentiellement des valeurs de d et de n. On peut ainsi associer à chaque système physique une « classe d'universalité » (d, n).
L’évolution du modèle d’Ising
Le modèle d’Ising, bien qu'il corresponde à une très grande simplification de la situation physique réelle, se révèle ardu à résoudre ; des solutions rigoureuses ne sont obtenues que dans des cas très simples. C'est ainsi que Lev Landau établit qu'il ne peut apparaître un ordre à grande distance sur un réseau à une seule dimension (d = 1). Lars Onsager calcule en 1944 l'aimantation du modèle d'Ising dans un plan (d = 2 et n = 1) au moyen d'une méthode mathématique complexe ; mais une approche générale n'est proposée qu'en 1972, par Kenneth Wilson, qui obtient le prix Nobel de physique en 1982 pour son travail sur la méthode dite du « groupe de renormalisation ». Il montre que le comportement de l'ordre est le même dans des systèmes aussi différents que les matériaux magnétiques, les mélanges liquide-gaz ou les cristaux liquides. C'est une confirmation remarquable de la justesse de l'approche proposée par Ising : les objets microscopiques peuvent être décrits de façon rudimentaire, car c'est la géométrie du système qui détermine seule les propriétés essentielles du diagramme de phase.
L'ordre cristallin
La plupart des corps purs adoptent un état cristallin à basse température. Les atomes sont disposés dans le cristal en un motif qui est répété périodiquement ; cette disposition parfaitement régulière détermine des propriétés électroniques, optiques et mécaniques bien précises. En raison de la périodicité des cristaux, il est possible de prévoir ces propriétés grâce aux outils théoriques de la physique des solides, mis en œuvre dès les années 1930. De nombreuses applications en électronique sont issues de ces travaux. Un domaine particulièrement notable est celui des semi-conducteurs : une page de notre civilisation est tournée avec la publication du principe du transistor à pointes par John Bardeen et Walter H. Brattain en 1948, qui reçoivent avec William B. Shockley le prix Nobel de physique en 1956 pour la réalisation, en 1951, du premier transistor à jonctions.
Les molécules peuvent également former des cristaux moléculaires en obéissant à des règles de compacité maximale. Cette possibilité de cristalliser permet de connaître la structure des molécules biologiques : c'est, par exemple, en étudiant aux rayons X des cristaux constitués de molécules d'ADN que James D. Watson et Francis C. Crick réussissent en 1953 à déterminer la structure en double hélice de ces longues chaînes qui portent le code génétique des êtres vivants.
Les cristaux liquides
Les cristaux liquides combinent certaines propriétés des liquides et certaines propriétés des solides cristallins : ce sont des liquides constitués de molécules organiques de forme particulière et qui peuvent adopter une orientation bien précise (les mousses de savon et certaines membranes cellulaires sont des cristaux liquides). L'orientation des molécules n'est pas aussi parfaite que dans un solide cristallin, mais elle suffit pour conférer au liquide des propriétés optiques utilisables pour les affichages.
Il existe une grande variété de familles de cristaux liquides. La famille des nématiques, constitués de molécules allongées en forme de bâtonnets, est généralement utilisée pour les écrans. Le principe d'affichage repose sur la possibilité de commander par une tension électrique le passage de l'état orienté polarisant la lumière à l'état désorganisé de liquide ordinaire non polarisant. Le prix Nobel a été attribué en 1991 au physicien Pierre-Gilles de Gennes pour ses travaux sur les cristaux liquides.
Une exception : supraconductivité et superfluidité
Une magnifique exception dans cette présentation des états ordonnés est constituée par les états superfluides : la supraconductivité et la superfluidité. Il s'agit là d'une des rares manifestations d'un effet quantique à l'échelle macroscopique.
L'état supraconducteur
Les propriétés des supraconducteurs sont spectaculaires : disparition totale de la résistance au passage du courant électrique, accompagnée par une expulsion du flux magnétique, et ce au-dessous d'une température critique qui dépend du matériau. Cette propriété n'est pas exceptionnelle : depuis la découverte en 1911 de la supraconductivité du mercure par Kamerlingh Onnes et Gilles Holst, des centaines de matériaux supraconducteurs ont été synthétisés. Mais elle heurte l'intuition des physiciens, car elle semble contraire au principe d'impossibilité du mouvement perpétuel : un courant installé dans un anneau supraconducteur peut s'y maintenir pendant des milliards d'années. Aucune description du mécanisme microscopique de la supraconductivité ne fut proposée avant qu'en 1956 John Bardeen, Leon N. Cooper et John Robert Schrieffer n'élaborent enfin une théorie de la supraconductivité (nommée théorie BCS), rapidement corroborée et adoptée par la communauté des physiciens.
Selon cette théorie, certains électrons forment des paires, les paires de Cooper, sous l'effet d'une force d'attraction, laquelle correspond dans le formalisme quantique à l'émission et à l'absorption par les électrons de vibrations des ions du réseau cristallin. Les paires d'électrons, contrairement aux électrons isolés, ont la faculté de participer collectivement à une onde quantique qui peut s'étendre sur des distances macroscopiques. Cette onde, qui peut transporter un courant électrique sans qu'il rencontre de résistance, est assez robuste ; elle résiste ainsi à la chaleur, tant que la température reste inférieure à la valeur critique ; elle résiste aussi au champ magnétique et aux défauts cristallins : des matériaux amorphes ou liquides peuvent être supraconducteurs.
La théorie BCS a entraîné de nombreux progrès théoriques et expérimentaux, mais l'état supraconducteur n'était observé qu'à très basse température. Dans les années 1970, le matériau supraconducteur présentant la température critique la plus haute (23 K) était le composé Nb3Ge. L'opinion générale des physiciens était alors que, pour des raisons fondamentales, la température critique de l'état supraconducteur ne pouvait probablement pas dépasser 30 K. En 1986, Georg Bednorz et Alexander Müller atteignent précisément cette température avec le composé LaBaCuO ; un an plus tard est synthétisé YBa2Cu3O7, qui atteint 92 K ; et, en 1988, Tl2Ba2Cu3O10, un matériau de la même famille des cuprates, avec une température critique de 125 K. Actuellement, il semble que la substitution du mercure dans ce composé permettrait d'atteindre 135 K, et que des cuprates supraconducteurs fabriqués couche atomique par couche atomique pourraient atteindre – et peut-être dépasser – une température critique de 250 K.
La superfluidité
L'hélium est le seul fluide qui ne se solidifie pas à basse température. L'hélium liquide présente alors la propriété étonnante de pouvoir s'écouler sans viscosité, donc sans le moindre frottement. La superfluidité, comme la supraconductivité, semble permettre un mouvement perpétuel « interdit » par la physique. Les deux phénomènes physiques sont décrits par le même mécanisme, qui s'applique cette fois aux noyaux d'hélium et non plus aux électrons. Les analogies sont ainsi nombreuses entre supraconducteurs et superfluides.
Les défauts
Les propriétés de la matière ordonnée sont souvent déterminées par les défauts de l'ordre, dont la grande variété interdit une présentation complète de leurs effets. Les trois cas suivants montrent les effets des impuretés dans les semi-conducteurs, des lignes de dislocation dans les solides et des parois dans les matériaux magnétiques. Nous avons déjà mentionné l'effet d'une très faible concentration d'impuretés (un atome étranger pour 100 millions d'atomes) sur la conductivité d'un semi-conducteur. Un atome étranger est un défaut ponctuel, mais on peut observer également des défauts sous forme de lignes ou de parois. Une ligne de dislocation est réalisée par l'interruption brutale d'un plan atomique dans un cristal ; grâce à la présence des dislocations, les cristaux de métal sont étonnamment malléables tant qu'ils n'ont pas été fortement déformés ; au contraire, après des déformations importantes, les dislocations sont enchevêtrées et ne peuvent plus se déplacer : on dit que le matériau est écroui. De même, l'aimantation macroscopique d'un métal comme le fer peut varier très facilement par le mouvement de parois qui séparent des domaines d'aimantations opposées ; une façon d'obtenir des aimants puissants et stables est d'agréger de petits grains magnétiques ne contenant qu'un seul domaine : ces matériaux sont les ferrites, couramment utilisées pour les fermetures de portes.
Cependant, les états de la matière étendue, homogène et en équilibre thermodynamique n'ont pas la diversité des états de la matière hors de ces conditions. La matière sous la forme d'objets de petite taille présente en effet des états différents de ceux de la matière étendue : par exemple, les quasi-cristaux à symétrie pentagonale ou bien les petits grains qui sont constitués d'un seul domaine magnétique. La matière peut aussi se présenter sous la forme de minces films, comme les bulles de savon, ou de fibres aux propriétés physiques très différentes de celles qu'elle possède lorsqu'elle se présente comme un volume.
La matière hétérogène
Une infinie variété d'états naturels et artificiels
Les combinaisons de ces formes (bulle, graine, fibre, lamelle…) dans des mélanges désordonnés ou bien des structures ordonnées conduisent à une infinie variété d'états de la matière hétérogène. L'hétérogénéité peut être liée à l'histoire du matériau (roches poreuses, boues, ciments, matériaux composites…) ou à un état d'équilibre (microémulsions, supraconducteurs contenant des fluxons magnétiques…). La structure géométrique des systèmes hétérogènes est aussi importante que la structure microscopique de l'ordre dans la matière homogène. Les systèmes granulaires présentent des comportements complexes particulièrement utiles à décrire pour prévoir le comportement des sols, éventuellement des avalanches. La matière fibrée, feuilletée, poreuse, les suspensions et les gels dans les liquides… illustrent des états et des comportements qui montrent l'imagination sans mesure de la nature, ou celle des hommes lorsque ces matériaux sont artificiels.
L'état vivant : structuration spontanée de systèmes ouverts ?
La matière se trouve souvent dans un état déterminé par son histoire ou par des conditions thermodynamiques hors de l'équilibre. La dynamique des changements d'état et les mécanismes de la croissance de l'ordre cristallin conduisent à des formations caractéristiques telles que des dendrites, des précipités, des agrégats de forme fractale, etc. Une autre caractéristique des états où la matière n'est pas au point d'équilibre est qu'elle s'organise et se structure spontanément. Dans les systèmes qui consomment de l'énergie (systèmes ouverts), le deuxième principe de la thermodynamique se traduit en effet par une tendance à réduire au minimum la production de désordre (entropie) par unité de temps, comme cela a été démontré de façon générale par Ilya Prigogine. Ce mécanisme est, entre autres, à l'origine de certaines formations nuageuses que l'on peut parfois observer (rouleaux régulièrement disposés parallèlement les uns aux autres). Il résout également le paradoxe – apparent – de la possibilité que présentent les systèmes vivants d'augmenter la complexité de leur organisation au cours du temps. Le paradoxe n'en est en fait pas un : les systèmes vivants ne sont pas contraints d'augmenter leur entropie, car ils ne sont pas isolés (si on isole un système vivant, il est bien connu qu'il finit par se dégrader irréversiblement). Les organismes vivants sont des systèmes ouverts, qui consomment de l'énergie en permanence. S'ils peuvent ainsi se structurer spontanément, d'après les résultats obtenus par Ilya Prigogine, il est difficile de savoir si ce mécanisme suffit à rendre compte de l'apparition de la vie sur notre planète, comme le suggèrent certains.





