lanthanide

Nom générique des éléments des terres rares, doués de propriétés chimiques très voisines, et dont le premier est le lanthane. (Ils sont souvent représentés par le symbole Ln.)
Lanthanides et terres rares
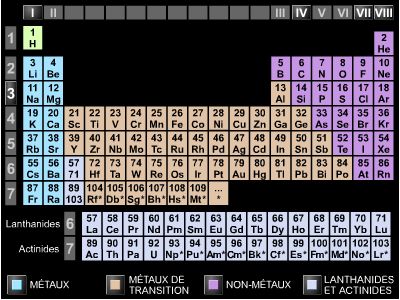
Les lanthanides comprennent le lanthane et les 14 éléments chimiques qui le suivent dans le tableau de classification périodique des éléments (numéros atomiques allant de 57 à 71). On les classe dans le tableau de Mendeleïev avec la série des actinides. Le chimiste suédois Jöns Jacob Berzelius (1779-1848) a séparé les lanthanides en deux sous-groupes suivant la solubilité de leurs sulfates : le groupe du cérium, qui rassemble le lanthane, le cérium, le praséodyme, le néodyme, le prométhéum et le samarium (éléments de numéros atomiques Z = 57 à 63, ou terres cériques) ; et le sous-groupe de l'yttrium, qui comprend l'europium, le gadolinium, le terbium, le dysprosium, l'holmium, l'erbium, le thulium, l'ytterbium et le lutécium (éléments de numéros atomiques allant de Z = 64 à 71, ou terres yttriques). Tout en formant un autre sous-ensemble de terres rares, le scandium et l'yttrium, de formules électroniques comparables, présentent peu de différences avec les lanthanides et sont le plus souvent étudiés ensemble.
Malgré un qualificatif dû à leur découverte tardive et aux difficultés à les séparer, les terres rares sont significativement présentes dans l'écorce terrestre : les réserves mondiales sont estimées à 45 Mt et, à titre d'exemples, le lanthane et le néodyme sont plus abondants dans la nature que le plomb, et le cérium est aussi répandu que l'étain ou le zinc. Les terres rares n'existent pas à l'état individuel mais en mélange dans plus de 150 minerais répertoriés, dont aucun ne présente la même répartition. La consommation mondiale de terres rares exprimée en oxydes est estimée à 25 000 t/an.
Configurations électroniques et propriétés chimiques
Les terres rares ont toutes la même configuration électronique externe et, de ce fait, des propriétés chimiques très voisines. Les lanthanides ne diffèrent que par la structure d'une couche plus interne : ce sont des éléments dits de transition interne. Cette particularité explique leur regroupement et fait qu'ils possèdent des propriétés physiques et chimiques analogues. Leur grande affinité pour l'oxygène se traduit par une pyrophoricité importante du métal ainsi que par la grande stabilité de la liaison terre rare/oxygène (formation d'oxydes très réfractaires). Les terres rares se combinent aisément aux anions pour donner des sels, solubles (chlorures, nitrates) ou insolubles (sulfures, fluorures, carbonates, oaxaltes, phosphates) ; elles peuvent être mises en jeu dans un grand nombre de composés minéraux de synthèse (borates, molybdates, silicates) et sont également facilement chélatées (liées à deux ou plusieurs sites distincts d'un même ligand) par des molécules organiques pour former des complexes très stables.
Méthodes d'extraction
Aucun développement technologique des terres rares n'aurait été possible sans des techniques de séparation très élaborées, rendues nécessaires par la similitude des propriétés chimiques des éléments à isoler.
Les cristallisations fractionnées utilisées au début du xxe siècle, puis les méthodes utilisant les résines échangeuses d'ions ont permis l'accès aux différentes terres rares avec des puretés satisfaisantes et se sont accompagnées des premières applications industrielles (manchons à incandescence, pierres à briquet, applications verrières et métallurgiques). Les exigences des marchés, en qualité et tonnages, ont justifié la mise en pratique de méthodes d'extraction par solvant. Elles ont permis l'obtention industrielle des oxydes ou sels des terres rares avec des puretés de plus en plus élevées (> 99,99 %), indispensables pour les applications en optique.
Les lanthanides de faible numéro atomique, c'est-à-dire les plus légers, se rencontrent essentiellement dans les minéraux de monazite (LnPO4) ; les plus lourds sont extraits surtout de la gadolinite. Le prométhium, qui ne possède que des isotopes radioactifs, a été séparé des produits de fission de l'uranium 235. Leurs propriétés physiques et chimiques étant très voisines, leur séparation est difficile. Elle se fait principalement par cristallisation fractionnée, échange d'ions sur résine et extraction par solvant. Les métaux sont obtenus soit par électrolyse des chlorures fondus, soit par réduction des chlorures ou des fluorures anhydres, respectivement par le sodium (pour les lanthanides légers) ou le magnésium (pour les lanthanides lourds). Ils sont ensuite purifiés par distillation. Aucun développement technologique des terres rares n'aurait été possible sans des techniques de séparation très élaborées, rendues nécessaires par la similitude des propriétés chimiques des éléments à isoler.
Applications industrielles
Les grandes applications industrielles mettent en œuvre des terres rares de nature et de spécificités fort différentes.
En métallurgie, leur rôle principal est celui de piège à oxygène, soufre ou autres éléments délétères pour les propriétés des fontes ou des aciers. Très souvent employées comme additifs structuraux, elles permettent aussi de contrôler la morphologie des inclusions de sulfures dans les aciers et la sphéroïdisation des impuretés de graphite dans les fontes (amélioration de la ductilité des matériaux ainsi que de leur résistance thermique ou mécanique).
Dans le domaine de la catalyse, les propriétés chimiques des terres rares leur confèrent un intérêt considérable pour améliorer la stabilité, l'activité ou la sélectivité des systèmes catalytiques. Ainsi, les catalyseurs multifonctionnels permettant de réduire les teneurs des gaz d'échappement en monoxydes de carbone et d'azote et en hydrocarbures sont constitués de métal précieux déposé sur un support d'alumine comportant de l'oxyde de cérium. L'oxyde de cérium, dans des teneurs de l'ordre de 20 % en poids, joue le rôle, grâce à ses propriétés oxydoréductrices, de régulateur de la teneur en oxygène du mélange gazeux (meilleure activité catalytique globale).
Les applications industrielles des terres rares dans le domaine de la céramique et du verre sont très variées : obtention de pourpres (néodyme), de verts (praséodyme) ou de roses (erbium) dans les verres de cristallerie ou ophtalmiques ; le cérium combiné au titane permet de réaliser un jaune vif, très utilisé pour les articles de table, mais son utilisation principale s'effectue dans le domaine de la décoloration : il oxyde certaines impuretés colorées (fer divalent) ou, du fait de sa forte absorption des ultraviolets et des électrons, évite le noircissement des verres sous l'effet de ces radiations (vitres, bouteilles, verres de lunettes soumis en permanence aux ultraviolets, faces avant de tubes télévision ou fenêtres sous rayonnements de haute énergie). Quant au lanthane, il permet l'obtention de verres boratés à haut indice de réfraction et faible dispersivité, indispensables en optique de précision pour la réalisation d'objectifs photographiques ou de lentilles de microscopes par exemple.
Les émissions luminescentes quasi monochromatiques sont mises à profit pour l'obtention de performances exceptionnelles en télévision, éclairage ou radioluminescence. Les luminophores aux terres rares utilisés pour l'éclairage ont permis la réalisation de tubes fluorescents trichromatiques : la radiation ultraviolette, émise par des gouttelettes de mercure excité entre deux électrodes, est transformée en lumière visible au moyen de trois luminophores dont les activateurs émettent chacun une des couleurs fondamentales (europium divalent pour le bleu et trivalent pour le rouge, terbium pour le vert). Les rendements lumineux et les durées de vie de ces tubes sont plusieurs fois supérieurs à ceux des lampes à incandescence traditionnelles.
En radioluminescence, une absorption intense des rayons X, un excellent rendement de conversion en lumière visible et une longueur d'onde d'émission bien adaptée à la sensibilité maximale des émulsions photographiques utilisées font des luminophores aux terres rares les matériaux de choix dans les écrans utilisés pour transformer une image radiologique médicale en image optique.
Les propriétés magnétiques exceptionnelles obtenues dans des alliages « élément de transition/terre rare » sont mises en œuvre dans les aimants permanents (SmCo5, Sm2Co17, Nd2Fe14B). La plus spectaculaire conséquence de leur utilisation a été la miniaturisation des aimants, ce qui s'est traduit en haute fidélité (Sm2Co17) par une diminution considérable du volume des haut-parleurs ou des micros (casques de baladeurs, notamment). D'autre part, le faible coût et les excellentes propriétés magnétiques des aimants au néodyme en font des matériaux prometteurs pour le remplacement des électroaimants (en particulier dans l'industrie automobile pour remplacer les bobinages).





