alcènes (suite)
Propriétés physiques
Il convient d’abord de rappeler (v. stéréochimie) que l’alcène le plus général
peut se présenter sous deux formes non spontanément interconvertibles, chaque fois que l’on a simultanément R1 ≠ R2 et R3 ≠ R4 ; ces formes sont appelées cis et trans, et sont représentées ainsi :
Cela tient à ce que les deux carbones éthyléniques et les atomes qui leur sont directement reliés sont dans un même plan et forment un ensemble rigide. Les isomères cis et trans ont des propriétés vulgaires très voisines, mais peuvent être différenciés par analyse spectrale (infrarouge, résonance magnétique nucléaire).
Les alcènes absorbent dans l’ultraviolet vers 1 850 Å et dans l’infrarouge entre 1 623 cm–1 (éthylène) et 1 680 cm–1 (éthylènes tétrasubstitués).
Les points d’ébullition des alcènes sont voisins de ceux des alcanes de même squelette. L’état solide est tout à fait exceptionnel à la température ambiante.
La densité et l’indice de réfraction sont un peu plus élevés que chez les alcanes. La solubilité dans l’eau est plus grande, quoique encore très faible. Par contre, à l’inverse des alcanes, les alcènes sont solubles dans SO2 liquide (il s’agit d’une addition réversible, parfois utilisée à la séparation d’un mélange alcanes-alcènes).
Propriétés chimiques
Le caractère essentiel des alcènes est la non-saturation. L’éthylène ne donne jamais lieu à substitution avant la disparition de la liaison double. C’est moins absolu pour ses homologues, mais, en aucun cas, la substitution ne porte sur les carbones éthyléniques.
Par exemple, à 600 °C :
La liaison éthylénique peut subir de nombreuses additions ; la plus simple est l’hydrogénation en alcane ; elle ne peut guère être réalisée que par voie catalytique (Ni, Pt). Le chlore et le brome s’additionnent aisément, mais l’iode difficilement :
Certains oxydants, KMnO4 dilué, OsO4 + H2O2, CF3—CO3H, conduisent à des α-glycols :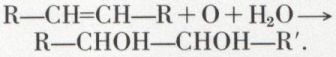
Pour toutes ces additions symétriques, la question du sens de l’addition sur un alcène symétrique ne se pose qu’au point de vue stéréochimique. On dit qu’il y a trans-addition du brome, ce qui s’exprime ainsi :
Mais l’addition de 2 OH au permanganate est une cisaddition.
Par contre, les alcènes subissent des additions dissymétriques obéissant à la règle de Markovnikov : le radical le plus négatif (le nucléophile) se fixe sur le carbone le plus substitué :
Les oxacides s’additionnent de deux façons ; avec H2SO4 concentré, on a surtout
L’hydroxyle régénère H2SO4, et l’alcool R—CHOH—CH3.
Les acides hypohalogéneux se comportent différemment :
L’oxydation permanganique poussée rompt la molécule en acides ou en cétones :
L’ozone s’additionne en un ozonide (explosif), dont l’hydrolyse conduit à des aldéhydes ou à des cétones :

Ces dégradations permettent de localiser la double liaison dans le squelette de l’alcène.
Les acides et les alcalis très forts provoquent la « migration » de la double liaison, le plus souvent vers l’intérieur de la chaîne :
L’une des propriétés les plus intéressantes des alcènes est leur polymérisation indéfinie, catalysée par les acides, le sodium, l’éthyl-aluminium ; dans le cas de l’éthylène, on aboutit à une chaîne très longue appelée polythène :
Le polythène est un verre organique très inerte ; les hauts polymères d’autres alcènes constituent des fibres synthétiques ou des résines et parfois des élastomères.
C. P.
S. Patai (sous la dir. de), Chemistry of Alkenes (New York, 1964).




