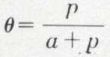Fixation d’un corps (l’adsorbat) à la surface d’un autre corps (l’adsorbant).
On appelle désorption le phénomène inverse. L’adsorption est très générale, car elle est due aux forces d’attraction qu’exercent à l’extérieur les molécules superficielles. L’adsorbant peut être liquide : dans une solution de savon, l’eau adsorbe les molécules d’acide gras formé, par hydrolyse, en une couche monomoléculaire dont les molécules ont leur chaîne carbonée perpendiculaire à la surface, le groupement terminal —CO2H hydrophile orienté vers l’intérieur de la solution ; du fait de cette adsorption, la tension superficielle du liquide est abaissée, ce qui accroît le pouvoir mouillant et favorise la formation de mousse.
Quand l’adsorbant est un solide, l’adsorbat peut être un corps présent dans une solution : on connaît le pouvoir décolorant du charbon vis-à-vis des liquides organiques ; l’analyse chromatographique emploie aussi ce type d’adsorption.
L’adsorption des gaz par les solides est importante par ses applications ; on en distingue deux types : l’adsorption physique, ou physisorption, et l’adsorption chimique, ou chimisorption. La première ne se manifeste qu’aux basses températures et met en jeu des forces peu intenses, dites « de Van der Waals » ; la chaleur dégagée lors de l’adsorption est seulement de l’ordre de 5 kcal/mole. Cette adsorption croît avec la pression du gaz, diminue par élévation de température ; à température et pression données, un gaz est d’autant plus adsorbé qu’il est plus facilement liquéfiable. Suivant les cas, le gaz peut former à la surface du solide une couche mono- ou pluri-moléculaire. La chimisorption présente des caractères nettement différents : elle a lieu à des températures bien plus élevées que la précédente ; l’énergie d’adsorption est de l’ordre de 100 kcal/mole, ce qui montre que les forces qui s’exercent entre adsorbant et adsorbat sont comparables à celles qui interviennent dans les liaisons chimiques, et que ces corps forment, par dislocation de la molécule adsorbée, une combinaison superficielle, dite « d’adsorption ».
Quel que soit le type d’adsorption du gaz, lorsque la couche adsorbée est monomoléculaire, la fraction θ de la surface de l’adsorbant couverte par l’adsorbat varie à température constante en fonction de la pression p du gaz suivant l’expression
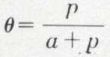
a étant constant à température donnée ; c’est l’isotherme de Langmuir.
La physisorption fournit un moyen de fractionnement en analyse immédiate et est aussi utilisée pour parfaire le vide dans une enceinte ; la chimisorption joue un rôle très important dans l’interprétation du mécanisme de la catalyse hétérogène.
Irving Langmuir
Physico-chimiste américain (Brooklyn 1881 - Falmouth 1957). Il a imaginé en 1913 les ampoules électriques à atmosphère gazeuse, construit en 1916 une pompe à vide moléculaire et découvert l’hydrogène atomique. Il est aussi l’auteur de travaux sur la chimie de surface et la catalyse. Prix Nobel de chimie pour 1932.
R. D.
S. Brunauer, The Adsorption of Gases and Vapours (Londres, 1944). / B. M. W. Trapnell, Chemisorption (Londres, 1955).