Corps simple métallique.
En 1789, l’Allemand Martin Heinrich Klaproth (1743-1817) obtint la zircone, dioxyde de zirconium, d’un minéral, le zircon (silicate de zirconium). C’est en 1824 que Berzelius* parvint à isoler le métal.
État naturel
On trouve dans la nature l’oxyde et le silicate. Le zirconium constitue 0,025 p. 100 de la lithosphère.
Atome
Le numéro atomique du zirconium est 40. C’est un élément de la deuxième série de métaux de transition. La structure électronique de l’état fondamental de l’atome est 1s2, 2s2, 2p6, 3s2, 3p6, 3d10, 4s2, 4p6, 4d2, 5s2. Les énergies successives des quatre premières ionisations ont les valeurs suivantes : 6,95 eV, 13,97 eV, 24,00 eV, 33,8 eV ; le rayon du cation Zr+4 est de 0,68 Å.
Corps simple
Le zirconium a une densité de 6,5. Il fond à 1 860 °C. Il possède de bonnes propriétés mécaniques, et sa faible section de capture des neutrons l’a fait employer dans l’industrie nucléaire pour le gainage des cartouches d’uranium. Ce métal réagit avec de nombreux corps simples. Il ne brûle qu’à haute température quand il est massif et dégage alors une forte chaleur de réaction. Pulvérulent, il brûle spontanément en présence de l’air.
Il est attaqué par l’acide sulfurique, l’eau régale et l’acide fluorhydrique. Il forme comme le titane des solutions solides interstitielles non stœchiométriques avec l’hydrogène. Les principaux minerais de zirconium étant un silicate et un oxyde, on les traite par le carbone et le chlore au rouge, et l’on obtient le tétrachlorure ZrCl4, qui est réduit ultérieurement par le magnésium.
Principaux dérivés
On connaît les chlorures de formules respectives ZrCl2, ZrCl3 et ZrCl4. Ce dernier est hydrolysé selon la réaction
ZrCl4 + H2O → ZrOCl2 + 2HCl.
On connaît des complexes dérivant des halogénures de zirconium, tels que (ZrCl4)3(POCl3)2,  ou encore K2ZrF6. Il existe aussi des complexes contenant l’anion
ou encore K2ZrF6. Il existe aussi des complexes contenant l’anion 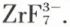 Les complexes bromés sont beaucoup moins stables que les complexes fluorés.
Les complexes bromés sont beaucoup moins stables que les complexes fluorés.
Les tétrachlorures et les tétrabromures de zirconium (comme ceux de titane) se comportent comme des acides de Lewis et, à ce titre, donnent des composés d’addition en particulier avec des composés oxygénés comme les alcools, les éthers et les composés carbonylés.
Le dioxyde de ZrO2 (zircone) est utilisé comme pigment. La zircone a un point de fusion élevé (2 700 °C) et est utilisée comme réfractaire. Cet oxyde, comme TiO2, peut s’unir à des oxydes basiques en donnant des zirconates, qui, dans certains cas, sont des oxydes multiples plutôt que des sels ; ainsi, CaZrO3 a la structure de la pérovskite CaTiO3.
H. B.
W. Espe, Zirconium (en tchèque, Prague, 1952 ; trad. all., Fussen, Bavière, 1953). / G. L. Miller, Zirconium (Londres, 1954 ; 2e éd., 1957).





 ou encore K2ZrF6. Il existe aussi des complexes contenant l’anion
ou encore K2ZrF6. Il existe aussi des complexes contenant l’anion 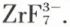 Les complexes bromés sont beaucoup moins stables que les complexes fluorés.
Les complexes bromés sont beaucoup moins stables que les complexes fluorés.