revêtement de surface (suite)
Les revêtements électrolytiques sont exécutés par des méthodes et dans des installations très diverses, suivant la nature du dépôt, la forme et les dimensions des pièces ainsi que l’importance des quantités à traiter : cuves isolées, cuves disposées en lignes, pièces disposées sur des montages ou placées en vrac dans des tonneaux immergés dans les bains, transfert manuel des pièces ou transfert automatique sur des machines de travail en continu (machines automatiques en carrousel ou machines à programmation avec les cuves disposées en long), installations de revêtement en continu de produits longs (feuillards, bandes, tôles, fils, tubes) par passage dans des cuves successives ou par traitement dit « hors cuves ». Les problèmes de revêtements électrolytiques font appel à des domaines scientifiques et techniques très variés : électrique et électrolytique (alimentation électrique, redresseurs de courant, étude de la répartition des potentiels électriques, rendement d’électrolyse, utilisation d’anodes solubles ou insolubles), physico-chimique et chimique (protection des cuves, chauffage, composition et analyse des bains, filtration, séchage, alimentation en eau déminéralisée, traitement final des effluents, ventilation, toxicité des produits) et mécanique (systèmes de transfert et montage des pièces, pompes, tuyauteries, construction de cuves et réservoirs).
Revêtement par réaction chimique de la surface avec une solution saline, un composé solide ou un gaz
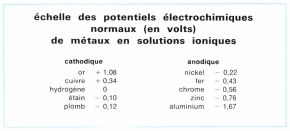
• Le revêtement par déplacement chimique d’un métal à partir d’un de ses sels en solution n’est possible que si le métal à revêtir est plus anodique ou plus électronégatif que le métal à déposer, ce qui est le cas du cuivrage de l’acier (réserve de cémentation, cuivrage de barres pour l’étirage), de l’étamage de l’aluminium ou de ses alliages (protection des pistons en alliage léger), du nickelage de l’acier, de la fonte, des cupro-alliages et des alliages d’aluminium (procédé Kanigen de nickelage chimique par dépôt d’une couche de nickel chargée en phosphore, dure, adhérente et résistant à l’abrasion), de l’argenture des cupro-alliages.
• Le traitement de coloration des métaux consiste à former en surface une mince pellicule d’oxyde, de sulfure, de carbonate, dont l’action protectrice est souvent limitée.
• Le traitement chimique superficiel fait appel à la formation d’oxydes ou de sels protecteurs. Parmi les procédés utilisés figurent notamment l’oxydation anodique de l’aluminium et de ses alliages (formation d’un revêtement d’alumine protecteur, facilement colorable par des vernis), la phosphatation de l’acier (dépôt protecteur, favorisant le frottement, à base de phosphates complexes de fer, de manganèse et de zinc), les traitements des alliages légers (dépôt de phosphates, de chromâtes, de fluorures d’aluminium complexes, qui servent de support à l’application de peintures et de vernis), les traitements divers de sulfuration des aciers ou des cupro-alliages, tels que le procédé de sulfinusation, dont la couche protectrice, à base de sulfure, de carbure, de carbonitrures de fer, est particulièrement appréciée pour ses qualités antigrippantes.
• Le traitement thermochimique utilise le principe de la diffusion superficielle à chaud d’un élément métallique. Dérivés du procédé de cémentation de l’acier par le carbone, les plus utilisés des traitements thermochimiques sur les alliages ferreux sont la calorisation, ou diffusion d’aluminium, la shérardisation, ou diffusion de zinc, et la chromisation, ou diffusion de chrome. Ce dernier procédé a reçu de nombreuses applications aéronautiques et aérospatiales pour les pièces devant résister à l’usure, à l’abrasion et à la corrosion à haute température.
Métallisation à chaud ou au trempé
L’immersion des pièces dans un bain de métal fondu se pratique depuis longtemps pour la protection des pièces ferreuses par étamage (« fer-blanc » employé à la confection des boîtes de conserve), par zincage ou galvanisation (« tôle galvanisée » pour toitures, ustensiles ménagers) et par dépôt d’alliage à base d’aluminium (procédé Sendzimir). Un décapage soigné de la surface du métal de base et l’emploi d’un flux approprié permettent le bon accrochage du revêtement sur son support.
Métallisation par projection au pistolet
Elle se pratique soit à partir de poudres, soit à partir de métal en fil, à l’aide d’un chalumeau oxyacétylénique par projection de gouttelettes de métal fondu sur la surface à revêtir ; ce procédé s’applique pour de nombreux métaux et alliages : zinc, étain, plomb, aluminium, alliages durs à base de nickel, de cobalt, de chrome, de tungstène (Stellites).
Métallisation sous vide ou par vapométallurgie
Cette méthode consiste à déposer une mince couche à partir de la vapeur métallique. On l’applique soit à des pièces, soit à des produits en continu, sous forme de dépôts d’aluminium, de zinc, de chrome, etc., dans les industries de l’électronique, de l’optique et de l’appareillage électrique.
Revêtement classique de matériaux non métalliques
On utilise surtout des peintures, des laques, des vernis, des émaux ainsi que des matières plastiques ; un procédé plus récent, le poudrage, se développe pour l’application de résines thermodurcissables pour le matériel domestique, les mobiliers de jardin, les carrosseries, etc., soit par application électrostatique au pistolet, soit par immersion des pièces dans un bain fluidisé de poudre.
La corrosion des métaux et leur protection
Causes de corrosion chimique et électrochimique (corrosion galvanique)
Elles sont nombreuses. Les principales sont :
— le milieu extérieur : nature, concentration chimique, impuretés, température, pression, renouvellement ou agitation, rayonnement lumineux, présence de courants électriques, conductibilité, etc. ;
— les facteurs propres au métal : composition, pureté, homogénéité, structure, état physico-chimique (traitement thermique, déformation), tensions internes ;
— la forme de la pièce et les conditions d’emploi : profil, état de surface (finition, aspérités, rayures), contact avec d’autres métaux, tensions, conditions d’immersion ou d’exposition, température de la pièce, etc.




