régulation (suite)
Le pH est une mesure de la concentration en ions 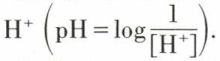 Le pH artériel est de l’ordre de 7,40 ; le pH veineux est voisin de 7,36, et le pH intracellulaire est estimé à 7. En ce qui concerne le pH artériel, des valeurs comprises entre 7,35 et 7,45 restent dans le domaine physiologique ; des valeurs inférieures à 7 et supérieures à 7,7 sont incompatibles avec la vie. L’activité des enzymes dépendant étroitement de la concentration en ions H+, le maintien du pH dans une zone relativement restreinte est particulièrement important.
Le pH artériel est de l’ordre de 7,40 ; le pH veineux est voisin de 7,36, et le pH intracellulaire est estimé à 7. En ce qui concerne le pH artériel, des valeurs comprises entre 7,35 et 7,45 restent dans le domaine physiologique ; des valeurs inférieures à 7 et supérieures à 7,7 sont incompatibles avec la vie. L’activité des enzymes dépendant étroitement de la concentration en ions H+, le maintien du pH dans une zone relativement restreinte est particulièrement important.
L’organisme contient divers systèmes tampons qui atténuent dans un premier temps les variations éventuelles du pH. À côté de cette régulation « physico-chimique » existent des régulations physiologiques mettant en jeu le poumon et le rein.
Le système tampon le plus abondant dans le plasma est le système  Une relation lie le pH à la concentration de bicarbonates et à celle de CO2 exprimée en pression partielle ([CO2] = a p CO2, a étant le coefficient de dissolution du CO2 dans l’eau) :
Une relation lie le pH à la concentration de bicarbonates et à celle de CO2 exprimée en pression partielle ([CO2] = a p CO2, a étant le coefficient de dissolution du CO2 dans l’eau) :
pour le sang artériel,
Une diminution de  ou une augmentation de la pCO2 abaisse le pH (acidose) ; une augmentation des bicarbonates ou une diminution de la pCO2 élève le pH (alcalose). La concentration plasmatique en
ou une augmentation de la pCO2 abaisse le pH (acidose) ; une augmentation des bicarbonates ou une diminution de la pCO2 élève le pH (alcalose). La concentration plasmatique en 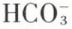 est sous la dépendance du rein ; la pCO2 artérielle est contrôlée par la ventilation.
est sous la dépendance du rein ; la pCO2 artérielle est contrôlée par la ventilation.
remarque. De la réaction de dissociation de l’acide carbonique  on tire
on tire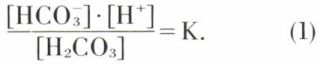
De la réaction d’hydratation
il vient
En remplaçant [H2CO3] par sa valeur dans l’équation (1), on obtient :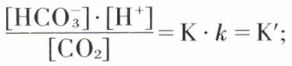
ou encore,
Sous forme logarithmique
l’équation s’écrit :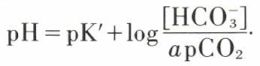
• Régulation ventilatoire. La pCO2 artérielle est égale à la pCO2 alvéolaire, qui dépend, elle-même, de la ventilation : une hyperventilation abaisse la pCO2 et, par suite, augmente le pH. En retour, la pCO2 et le pH contrôlent la ventilation. Il existe deux types de récepteurs : les récepteurs carotidiens, sensibles aux variations de la pCO2 artérielle et de la concentration en ions H+ ; les récepteurs centraux (bulbaires), sensibles uniquement au CO2. Une augmentation de la pCO2 ou une diminution du pH (augmentation de la concentration en ions H+) stimule la ventilation et inversement. Lorsque s’instaure une acidose due à un excès de composés acides dans la circulation (cétoacidose chez un diabétique par exemple), l’augmentation de la concentration en ions H+ stimule la ventilation, d’où une diminution de pCO2 qui tend à relever la valeur du pH (compensation ventilatoire de l’acidose). Mais la chute de pCO2 entraîne par elle-même une inhibition de la ventilation ; la ventilation s’équilibre à un niveau qui correspond à un compromis entre la stimulation par les ions H+ et l’inhibition due à la baisse de pCO2. Un tel antagonisme limite l’intensité de la compensation ventilatoire.
• Régulations rénales. Le rein participe au maintien de l’équilibre acido-basique par plusieurs mécanismes.
1. Sécrétion d’ions H+. La cellule du tubule rénal est capable de produire des ions H+ par un mécanisme encore bien mal connu ; ces ions sont sécrétés (transport actif) dans l’urine. Les ions OH– libérés se combinent avec le CO2 (réaction catalysée par l’anhydrase carbonique) pour former des ions HCO3– qui diffusent vers le plasma. La sécrétion d’ions H+ est présente dans la partie proximale du tubule, mais est plus importante dans la partie distale ; elle est fortement augmentée par l’acidose et au contraire réduite en cas d’alcalose.
2. Réabsorption des ions  Elle s’effectue essentiellement au niveau proximal. Les ions H+ sécrétés décomposent les bicarbonates on CO2 et H2O :
Elle s’effectue essentiellement au niveau proximal. Les ions H+ sécrétés décomposent les bicarbonates on CO2 et H2O :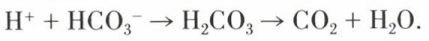
Le CO2 ainsi produit diffuse dans les cellules et participe à la formation de HCO3– sous l’action de l’anhydrase carbonique ; le bilan se traduit donc par un transfert des bicarbonates urinaires dans le plasma. Ce mécanisme est d’autant plus intense que la pCO2 est élevée (on en ignore la raison) ; dans ces conditions, une acidose due à un excès de CO2 dans le sang (acidose ventilatoire) sera compensée par une élévation de la concentration plasmatique en HCO3– d’où une remontée du pH. Certains auteurs ont suggéré que les ions H+ pouvaient être transportés directement au travers de la cellule, sans nécessairement passer par le cycle précédemment décrit, mais cette hypothèse ne paraît pas actuellement solidement étayée.
3. Excrétion des ions H+. L’urine définitive peut avoir un pH voisin de 4, mais la quantité d’ions H+ est beaucoup plus importante que ne le laisse supposer ce pH. Une partie de ces ions est excrétée sous forme de phosphates acides, une autre partie sous forme d’ions ammonium (NH4+). Les cellules tubulaires ont en effet la propriété de synthétiser de l’ammoniac à partir d’un acide aminé, la glutamine ; ce mécanisme revêt une certaine importance dans la mesure où la production de NH3 est stimulée lorsque le pli sanguin décroît et, au contraire, réduite lors d’une alcalose ; la production d’ammoniac est ainsi ajustée à la sécrétion des ions H+. Les modalités de la régulation de cette synthèse sont pratiquement inconnues.
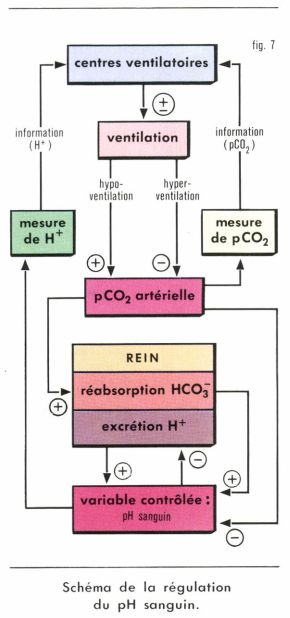
Un essai de synthèse des principales données concernant la régulation du pH sanguin est présenté sur la figure 7.
Régulation de la synthèse des protéines
La relation entre gènes et protéines est bien établie, et les récentes acquisitions de la génétique moléculaire permettent de se faire une idée relativement précise des principaux mécanismes responsables de la synthèse des protéines. Il est évident que cette synthèse ne peut être anarchique et doit nécessairement être modulée en fonction des besoins de l’organisme. L’étude de la régulation de la synthèse d’une protéine enzymatique, la galactosidase, chez une Bactérie (Escherichia coli), fournit un exemple particulièrement clair de cet aspect du problème de la synthèse protéique.
Le lactose peut constituer un nutriment de la Bactérie dans la mesure où il est hydrolyse par la β-galactosidase en galactose et en glucose. On a constaté que plus la concentration de lactose est élevée dans le milieu de culture, plus la quantité de β-galactosidase présente dans les Bactéries est grande. Cela suggère l’existence d’une relation étroite entre la synthèse d’enzyme et la quantité de substrat.




