photochimie (suite)
Christian Johann Dietrich, dit Theodor, baron von Grotthuss
Physicien allemand (Leipzig 1785 - Geddutz, Courlande, 1822). Il donna en 1805 une première théorie de l’électrolyse et énonça en 1818 la loi fondamentale de la photochimie.
Rendement quantique
C’est, dans une réaction photochimique, le rapport du nombre des molécules consommées à celui des quanta absorbés. Il peut être égal à 1, comme c’est le cas dans la formation de l’image latente photographique par exposition à la lumière d’une émulsion de bromure d’argent dans un support de gélatine.
Le mécanisme est simple, grossièrement résumé par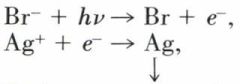
Br étant capté par la gélatine.
Le plus souvent, cependant, le rendement quantique est différent de 1. Cela est dû à ce que la phase primaire (photochimique) d’activation des molécules par les photons ne constitue pas en général à elle seule toute la réaction finalement observée ; des transformations secondaires non photochimiques, de nombre et de complexité variables selon les exemples, se produisent à partir des molécules directement activées par les photons dans la phase dite « lumineuse » de la réaction. Ces transformations secondaires sont de plusieurs sortes.
a) Les éléments activés par les photons peuvent jouer le rôle d’initiateurs dans une réaction en chaîne (v. cinétique). C’est le cas des atomes Cl dans la synthèse photochimique du chlorure d’hydrogène :
Cl2 + hν → 2 Cl*,
Cl* + H2 → HCl + H*,
H* + Cl2 → HCl + Cl*, etc. ;
à l’absorption d’un seul photon peuvent correspondre, l’expérience le montre, plus de 105 molécules transformées ; il s’agit, dans la phase secondaire, de réactions très exoénergétiques dont l’énergie d’activation est faible, circonstances favorables à l’entretien des chaînes.
b) L’activation primaire peut cesser par choc, par recombinaison d’éléments d’abord séparés, par émission d’un rayonnement de luminescence ; dans tous ces cas, le rendement quantique se trouve diminué ; en l’absence de chaînes, il est alors inférieur à 1, comme dans la photolyse endoénergétique de nombreux corps minéraux et organiques à température ordinaire.
L’assimilation chlorophyllienne, ou photosynthèse*, de mécanisme complexe, peut être globalement résumée suivant
n CO2 + n H2O → (CH2O)n + n O2,
réaction endoénergétique accompagnée d’une variation d’enthalpie ΔH = n.115 kcal ; compte tenu des zones d’absorption de la chlorophylle, on calcule aisément que trois photons au minimum sont nécessaires pour la transformation d’une molécule CO2 ; en fait, le rendement quantique, variable suivant les conditions, est inférieur à la limite précédente.
R. D.
N. J. Turro, Molecular Photochemistry (New York, 1965). / M. Mousseron-Canet et J. C. Mani, Photochimie et réactions moléculaires (Dunod, 1969). / R. P. Wayne, Photochemistry (Londres et New York, 1970). / R. B. Cundall et A. Gilbert, Photochemistry (Londres, 1971).





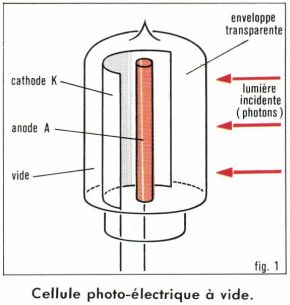
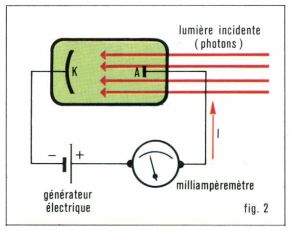
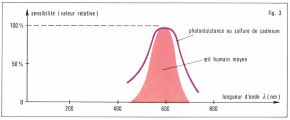
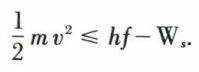

 En exprimant Ws en électrons-volts et λc en nanomètres, on trouve
En exprimant Ws en électrons-volts et λc en nanomètres, on trouve  Pour le césium, Ws = 1,9 eV ; donc λc = 650 nm (lumière rouge).
Pour le césium, Ws = 1,9 eV ; donc λc = 650 nm (lumière rouge).